题目内容
有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如图1所示: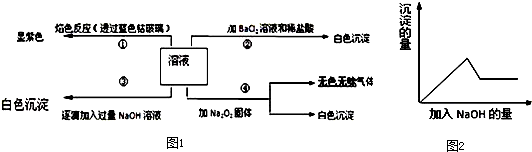
第③个实验中,生成白色沉淀的量与加入NaOH的量如图2所示的相互关系.据此可知:
(1)在原溶液中一定不存在的离子有
(2)在原溶液中一定存在的离子有
(3)写出第②第③个实验中发生反应的离子方程式
②

第③个实验中,生成白色沉淀的量与加入NaOH的量如图2所示的相互关系.据此可知:
(1)在原溶液中一定不存在的离子有
Fe3+、Fe2+、NH4+、Cu2+、CO32
Fe3+、Fe2+、NH4+、Cu2+、CO32
,(2)在原溶液中一定存在的离子有
Al3+、Mg2+、K+、SO42-
Al3+、Mg2+、K+、SO42-
(3)写出第②第③个实验中发生反应的离子方程式
②
SO42-+Ba2+═BaSO4↓
SO42-+Ba2+═BaSO4↓
③Mg2++2OH-=Mg(OH)2↓
Mg2++2OH-=Mg(OH)2↓
,Al3++3OH-=Al(OH)3↓
Al3++3OH-=Al(OH)3↓
,Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.分析:溶液透过蓝色钴玻璃焰色反应呈紫色,说明溶液中含有K+离子,溶液呈无色,则一定不含有色离子,逐滴加入过量NaOH溶液有白色沉淀,则溶液中含有Mg2+离子,
加入氯化钡和盐酸后生成白色沉淀,由于溶液中没有Ag+离子,则生成沉淀为BaSO4,溶液中含有SO42-离子,第③个实验中,生成白色沉淀的量与加入NaOH的量的先增大后减小,则说明溶液中含有Al3+离子.
加入氯化钡和盐酸后生成白色沉淀,由于溶液中没有Ag+离子,则生成沉淀为BaSO4,溶液中含有SO42-离子,第③个实验中,生成白色沉淀的量与加入NaOH的量的先增大后减小,则说明溶液中含有Al3+离子.
解答:解:溶液透过蓝色钴玻璃焰色反应呈紫色,说明溶液中含有K+离子,溶液呈无色,则一定不含Fe3+、Fe2+、Cu2+,逐滴加入过量NaOH溶液有白色沉淀,则溶液中含有Mg2+离子,一定不含CO32-,加入氯化钡和盐酸后生成白色沉淀,由于溶液中没有Ag+离子,则生成沉淀为BaSO4,溶液中含有SO42-离子,第③个实验中,生成白色沉淀的量与加入NaOH的量的先增大后减小,则说明溶液中含有Al3+离子,一定不含有铵根离子,综上可知:原溶液中一定含有Al3+、Mg2+、K+、SO42-,一定不含Fe3+、Fe2+、NH4+、Cu2+、CO32-,
(1)原溶液中一定不含有Fe3+、Fe2+、NH4+、Cu2+、CO32-,故答案为:Fe3+、Fe2+、NH4+、Cu2+、CO32-;
(2)原溶液中一定含有Al3+、Mg2+、K+、SO42-,故答案为:Al3+、Mg2+、K+、SO42-;
(3)溶液中含有SO42-,加入氯化钡发生的反应为:SO42-+Ba2+═BaSO4↓,含有Al3+、Mg2+,加入氢氧化钠发生的反应有:Mg2++2OH-=Mg(OH)2↓,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,
故答案为:SO42-+Ba2+═BaSO4↓;Mg2++2OH-=Mg(OH)2↓;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O.
(1)原溶液中一定不含有Fe3+、Fe2+、NH4+、Cu2+、CO32-,故答案为:Fe3+、Fe2+、NH4+、Cu2+、CO32-;
(2)原溶液中一定含有Al3+、Mg2+、K+、SO42-,故答案为:Al3+、Mg2+、K+、SO42-;
(3)溶液中含有SO42-,加入氯化钡发生的反应为:SO42-+Ba2+═BaSO4↓,含有Al3+、Mg2+,加入氢氧化钠发生的反应有:Mg2++2OH-=Mg(OH)2↓,Al3++3OH-=Al(OH)3↓,Al(OH)3+OH-=AlO2-+2H2O,
故答案为:SO42-+Ba2+═BaSO4↓;Mg2++2OH-=Mg(OH)2↓;Al3++3OH-=Al(OH)3↓;Al(OH)3+OH-=AlO2-+2H2O.
点评:本题考查物质的推断,题目难度不大,正确推断离子组的成分为解答本题的关键,注意离子的特征离子反应.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目

 所示的相互关系。据此可知:
所示的相互关系。据此可知:


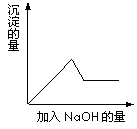 第③个实验中,生成白色沉淀的量与加入NaOH的量有右图
第③个实验中,生成白色沉淀的量与加入NaOH的量有右图
 所示的相互关系。据此可知:
所示的相互关系。据此可知: