题目内容
 如图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况.达到平衡后,改变压强,平衡不移动.下列说法中正确的是( )
如图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况.达到平衡后,改变压强,平衡不移动.下列说法中正确的是( )| A、Z物质的变化情况为曲线b |
| B、该反应的化学方程式为:2X(g)?3Y(g)+Z(g) |
| C、0→t1,X的物质的量浓度变化量为1.2mol/L |
| D、若t1=1min,则v(Y )=0.02mol?L-1?s-1 |
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以Z为反应物,不是生成物,Z的物质的量减小,据此判断;
B、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以方程式为2X(g)+Z(g)?3Y(g),据此判断;
C、0→t1,X的物质的量浓度变化量为2.0mol/L-1.2mol/L=0.8mol/L,据此判断;
D、根据v=
计算.
B、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以方程式为2X(g)+Z(g)?3Y(g),据此判断;
C、0→t1,X的物质的量浓度变化量为2.0mol/L-1.2mol/L=0.8mol/L,据此判断;
D、根据v=
| △c |
| △t |
解答:
解:A、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以Z为反应物,不是生成物,Z的物质的量减小,故A错误;
B、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以方程式为2X(g)+Z(g)?3Y(g),故B错误;
C、0→t1,X的物质的量浓度变化量为2.0mol/L-1.2mol/L=0.8mol/L,故C错误;
D、根据v=
可知,v(Y )=
=
=0.02mol?L-1?s-1,故D正确;
故选D.
B、达到平衡后,改变压强,平衡不移动,所以该反应是前后数气体计量数不变的反应,根据反应中物质的量之比等于计量数之比,设容器为1L,则△n(X)=0.8mol,△n(Y)=0.8mol,△n(Z)=0.8mol,因为前后计量数相等,所以方程式为2X(g)+Z(g)?3Y(g),故B错误;
C、0→t1,X的物质的量浓度变化量为2.0mol/L-1.2mol/L=0.8mol/L,故C错误;
D、根据v=
| △c |
| △t |
| 1.2mol/L |
| 1min |
| 1.2mol/L |
| 60s |
故选D.
点评:本题主要考查了根据浓度的变化写化学方程式以及速率的计算,难度不大,解题关键在基础知识的运用.

练习册系列答案
相关题目
向盛有KI溶液的试管中加入一定量CCl4后,滴加少量氯水,振荡,CCl4层变成紫色,继续滴加氯水,振荡,CCl4层颜色会逐渐变浅直至无色.下列说法正确的是( )
| A、CCl4层显紫色是因为有I2生成 |
| B、溶液分两层,紫色层在上层 |
| C、CCl4层显紫色是因为有Cl2生成 |
| D、CCl4层颜色最终会变为无色因为I2会升华 |
下列关于名称与化学用语表述正确的是( )
| A、乙稀:CH2=CH2 |
| B、过氧化氢:H2O |
| C、乙醇:CH3CHO |
| D、乙酸:CH3COOH |
已知反应X+Y=M+N为吸热反应,对该反应的下列说法中正确的是( )
| A、X的能量一定低于M的能量 |
| B、Y的能量一定低于N的能量 |
| C、因该反应为吸热反应,故该反应一定要加热才可发生 |
| D、X和Y的总能量一定低于M和N的总能量 |
实验室制取下列气体的实验正确的是( )
A、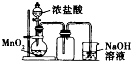 实验室制氯气 |
B、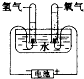 实验室制氧气 |
C、 实验室制氨气 |
D、 实验室制二氧化碳 |
1molCH4与一定量的氯气在光照条件下发生取代反应,若产生的四种取代物的物质的量相等,则反应生成HCl的物质的量为( )
| A、1.25mol |
| B、2mol |
| C、2.5mol |
| D、4mol |
 某气态不饱和链烃CmHn 在镍的催化下跟氢气发生加成反应,生成产物CmHn+x.今取CmHn与氢气的混合气体共60mL进行实验,反应前混合气体中氢气体积为W(横坐标),反应后气体总体积为V(纵坐标),其相互关系如图所示:上述气体的体积均是在同温同压下测定,单位是mL.由此可知x的数据是( )
某气态不饱和链烃CmHn 在镍的催化下跟氢气发生加成反应,生成产物CmHn+x.今取CmHn与氢气的混合气体共60mL进行实验,反应前混合气体中氢气体积为W(横坐标),反应后气体总体积为V(纵坐标),其相互关系如图所示:上述气体的体积均是在同温同压下测定,单位是mL.由此可知x的数据是( )