题目内容
实验室常加热氯化铵与氢氧化钙固体制取氨气,写出该反应的化学方程式: ,可用 来检验氨气,现要制得2.24L(标况)氨气,理论上需要氯化铵固体 g.(相对原子质量:N-14 H-1Cl-35.5)
考点:铵盐,化学方程式的有关计算
专题:计算题,氮族元素
分析:氯化铵与氢氧化钙反应生成氯化钙、水和氨气;氨气水溶液呈碱性;依据Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O计算现要制得2.24L(标况)氨气,理论上需要氯化铵固体的质量.
| ||
解答:
解:氯化铵与氢氧化钙反应生成氯化钙、水和氨气,方程式为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O;
氨气水溶液呈碱性,可使红色石蕊试纸变蓝色,所以可以用湿润的红色石蕊试纸检验氨气;
依据方程式:
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
107g 44.8L
m 2.24L
解得m=5.35g;
故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O;湿润的红色石蕊试纸;5.35.
| ||
氨气水溶液呈碱性,可使红色石蕊试纸变蓝色,所以可以用湿润的红色石蕊试纸检验氨气;
依据方程式:
Ca(OH)2+2NH4Cl
| ||
107g 44.8L
m 2.24L
解得m=5.35g;
故答案为:Ca(OH)2+2NH4Cl
| ||
点评:本题考查了氨气的实验室制备和相关计算,题目难度不大,熟悉实验室制备氨气的原理和氨气的性质是解题关键.

练习册系列答案
相关题目
能表示阿伏加德罗常数数值的是( )
| A、1 mol 金属钠含有的电子数 |
| B、标准状况下,22.4 L 苯所含的分子数 |
| C、0.012 kg 12C所含的原子数 |
| D、1 L 1 mol?L-1硫酸溶液所含的H+数 |
 如图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况.达到平衡后,改变压强,平衡不移动.下列说法中正确的是( )
如图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况.达到平衡后,改变压强,平衡不移动.下列说法中正确的是( )| A、Z物质的变化情况为曲线b |
| B、该反应的化学方程式为:2X(g)?3Y(g)+Z(g) |
| C、0→t1,X的物质的量浓度变化量为1.2mol/L |
| D、若t1=1min,则v(Y )=0.02mol?L-1?s-1 |
下列有机实验操作或叙述正确的是( )
| A、将乙烯和乙炔气体分别通入溴的四氯化碳溶液中前者退色,后者不退色 |
| B、甲烷和氯气在室温下的黑暗环境中可以稳定存在 |
| C、苯能使溴水退色是因为二者反应生成了溴苯 |
| D、要除去乙烷中的乙烯制得纯净的乙烷,可将混合气通入酸性高锰酸钾溶液中 |
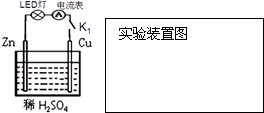 (1)原电池是一种将
(1)原电池是一种将 如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题:
如图为用惰性电极电解CuCl2溶液,并验证其产物的实验装置,回答下问题: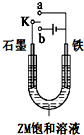 X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答:
X、Y、Z、W为按原子序数由小到大排列的四种短周期元素.已知:①X可分别与Y、W形成X2Y、X2Y2、XW等共价化合物;②Z可分别与Y、W形成Z2Y、Z2Y2、ZW等离子化合物.请回答: