题目内容
一定量的锌粉和6mol?L-1的过量盐酸反应,当向其中加入少量的下物质:①石墨 ②CuO ③铜粉 ④锌粒 ⑤浓盐酸 ⑥无水乙酸 ⑦KNO3溶液 ⑧CuCl2时,能够加快反应速率,又不响产生H2总量的是( )
| A、①③④ | B、①③⑤ |
| C、②④⑧ | D、①⑤⑦ |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:盐酸过量,则锌完全反应,锌的量决定氢气的体积,能够加快反应速率,又不影响产生H2的总量,采取措施有:形成原电池,注意形成原电池是不能消耗Zn,升高温度,改变锌粉的颗粒大小,增大氢离子的浓度等,以此来解答.
解答:
解:①加入石墨粉,构成原电池,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故①正确;
②加入CuO,与盐酸反应生成氯化铜,氯化铜与锌反应生成铜,形成原电池,加快反应,但与盐酸反应的锌的量减少,生成氢气的总量减少,故②错误;
③加入铜粉,构成原电池,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故③正确;
④加入铁粉,构成原电池,反应速率加快,锌反应完毕,铁可以与盐酸反应生成氢气,产生H2的总量增大,故④错误;
⑤加入浓盐酸,氢离子浓度增大,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故⑤正确;
⑥无水乙酸,氢离子浓度增大,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故⑥正确;
⑦KNO3溶液,在酸性条件下与锌反应生成NO,不生成氢气,影响生成氢气的总量,故⑦错误;
⑧加入CuCl2,锌置换铜,形成原电池反应,消耗锌,生成氢气的总量减少,生成氢气的速率增大,故⑧错误.
故选B.
②加入CuO,与盐酸反应生成氯化铜,氯化铜与锌反应生成铜,形成原电池,加快反应,但与盐酸反应的锌的量减少,生成氢气的总量减少,故②错误;
③加入铜粉,构成原电池,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故③正确;
④加入铁粉,构成原电池,反应速率加快,锌反应完毕,铁可以与盐酸反应生成氢气,产生H2的总量增大,故④错误;
⑤加入浓盐酸,氢离子浓度增大,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故⑤正确;
⑥无水乙酸,氢离子浓度增大,反应速率加快,不影响锌粉的量,不影响产生H2的总量,故⑥正确;
⑦KNO3溶液,在酸性条件下与锌反应生成NO,不生成氢气,影响生成氢气的总量,故⑦错误;
⑧加入CuCl2,锌置换铜,形成原电池反应,消耗锌,生成氢气的总量减少,生成氢气的速率增大,故⑧错误.
故选B.
点评:本题考查化学反应速率的影响元素,为高频考点,侧重于学生的分析能力的考查,注意加入氧化铜、Fe粉对氢气总量的影响,是本题的易错点,题目难度中等,

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
下列装置中能构成原电池的是( )
A、 |
B、 |
C、 |
D、 |
下列说法正确的是( )
| A、采用天然石材装修家居,可减轻室内甲醛等有机物和放射性物质的污染 |
| B、所有烷烃和蛋白质分子中都存在碳碳单键 |
| C、回收电子垃圾通过高温焚烧熔出金属,可实现资源循环利用和绿色环保 |
| D、乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 |
下列离子方程式不正确的是( )
| A、向100mL 0.1mol/L的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
| C、用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O═NaHCO3↓+NH4+ |
D、向水杨酸( )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: |
异戊烷和新戊烷互为同分异构体的依据是( )
| A、具有相似的化学性质 |
| B、具有相似的物理性质 |
| C、具有相同的空间结构 |
| D、分子式相同,但结构不同 |
下列离子方程式书写正确的是( )
| A、澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2═CaCO3↓+H2O |
| B、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、二氧化硅与烧碱溶液反应:SiO2+2OH-═SiO32-+H2O |
| D、硅酸和烧碱溶液中和:H++OH-═H2O |
SO2的回收利用方案如图所示.下列说法错误的是( )
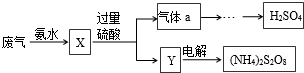

| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y中含NH4HSO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
在多电子原子中,轨道能量是由以下哪些因素决定( )
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子自旋状态.
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子自旋状态.
| A、①② | B、①④ | C、②③ | D、③④ |