题目内容
2.下列有关混合物的分离方法中,正确的是( )| A. | 从食盐溶液中获得食盐晶体采用降温结晶的方法 | |
| B. | 除去酒精中含有的少量水采用蒸馏的方法 | |
| C. | 除去氯化钠溶液中少量的泥沙用蒸馏的方法 | |
| D. | 从碘水中获得碘的晶体采用过滤的方法 |
分析 A.食盐溶于水,可将水蒸发掉得到NaCl;
B.酒精与水互溶,二者沸点不同;
C.泥沙不溶于水;
D.碘易溶于水.
解答 解:A.食食盐溶于水,从食盐溶液中获得食盐晶体采用蒸发的方法,故A错误;
B.酒精与水互溶,应利用加CaO后蒸馏除去酒精中含有的少量水,故B正确;
C.泥沙不溶于水,可用过滤的方法除杂,故C错误;
D.碘溶于水,不能利用过滤法分离,从碘水中获得碘的晶体应采用萃取、分液、蒸馏的方法,故D错误;
故选B.
点评 本题考查混合物分离、提纯实验方法的设计,为高频考点,把握物质的性质及分离原理为解答的关键,侧重蒸发、蒸馏、萃取、分液等分离方法的考查,题目难度不大.

练习册系列答案
相关题目
9.${\;}_{15}^{25}$P是我国最近合成的一种新核素,下列有关${\;}_{15}^{25}$P表示的磷原子的说法中正确的是( )
| A. | 核外有25个电子 | |
| B. | 是一种新元素 | |
| C. | 核内有15个质子,核外有10个电子 | |
| D. | 质量数为25,原子序数为15,核内有10个中子 |
10.如表为元素周期表的一部分,用元素符号或化学式回答下列问题.
(1)10种元素中,化学性质最不活泼的是Ar,除⑩外原子半径最大的是K.
(2)①②⑤三种元素最高价氧化物对应的水化物碱性最强的是KOH>NaOH>Al(OH)3
(3)①②③④⑤⑧六种元素形成的离子半径由大到小的顺序为S2->K+>Ca2+>Na+>Mg2+>Al3+
(4)元素⑦的氢化物的化学式为H2O;该氢化物和元素②单质反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)①⑨形成的化合物灼烧时火焰焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为2NaBr+Cl2=2KCl+Br2.
(6)③的单质在⑥⑦形成化合物中燃烧的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;单质⑨溶入⑥⑧形成化合物所得溶液的颜色为橙红色;⑧⑨形成氢化物的稳定性由强到弱顺序为HCl>HBr.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤三种元素最高价氧化物对应的水化物碱性最强的是KOH>NaOH>Al(OH)3
(3)①②③④⑤⑧六种元素形成的离子半径由大到小的顺序为S2->K+>Ca2+>Na+>Mg2+>Al3+
(4)元素⑦的氢化物的化学式为H2O;该氢化物和元素②单质反应的化学方程式为2K+2H2O=2KOH+H2↑.
(5)①⑨形成的化合物灼烧时火焰焰色为黄色;该化合物的溶液与元素⑧的单质反应的化学方程式为2NaBr+Cl2=2KCl+Br2.
(6)③的单质在⑥⑦形成化合物中燃烧的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C;单质⑨溶入⑥⑧形成化合物所得溶液的颜色为橙红色;⑧⑨形成氢化物的稳定性由强到弱顺序为HCl>HBr.
17.“纳米材料”是粒子直径为1~100nm的材料,纳米碳就是其中一种.将纳米碳均匀分散到蒸馏水中得到一种分散系,下列有关该分散系的说法错误的是( )
| A. | 属于溶液 | B. | 能产生丁达尔效应 | ||
| C. | 分散质粒子能透过滤纸 | D. | 纳米碳粒子能够发生布朗运动 |
7.下列说法不正确的是( )
| A. | 放热反应中反应物的总焓大于生成物的总焓 | |
| B. | 原子组成分子一定放出热量 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 化石燃料在地球上的蕴藏量是有限的,而且又都是经过亿万年才能形成的非再生资源 |
14.将A与B的混合物15mol放人容积为2L的密闭容器里,在一定条件下发生反应:2A(g)+3B(g)?C(g)+2D(g),经过15min达到平衡,达平衡时容器内的压强是反应前的$\frac{4}{5}$.则以B气体的浓度变化表示的反应速率是( )
| A. | 0.15mol•L-1•min-1 | B. | 0.3mol•L-1•min-1 | ||
| C. | 0.45mol•L-1•min-1 | D. | 0.6mol•L-1•min-1 |
 香精里面含有酯类物质,工业上以A为主要原料来合成酯C4H8O2,其合成路线如图所示.其中A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.又知2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.
香精里面含有酯类物质,工业上以A为主要原料来合成酯C4H8O2,其合成路线如图所示.其中A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平.又知2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH.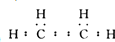
 .
. 碳碳双键 ②
碳碳双键 ② 羰基.
羰基.