题目内容
17.下列说法中不正确的是( )| A. | 反应是放热还是吸热要由反应物和生成物所具有的总能量来决定 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 若用50mL 0.55mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和 50mL 0.50mo1•L-1的硫酸充分反应,两反应测定的中和热是相等的 | |
| D. | 在101KPa时,1mol碳完全燃烧生成二氧化碳气体时放出的热量为碳的燃烧热 |
分析 A、根据反应物和生成物的能量大小可以判断反应的吸放热;
B、一个化学反应发生的条件与反应的热效应无关;
C、中和热均为稀的强酸、强碱反应生成1mol水放出的热量;
D、燃烧热是1mol可燃物质完全燃烧生成稳定氧化物放出的热量.
解答 解:A、反应物和生成物所具有的总能量决定了反应是放热还是吸热,反应物所具有的总能量大于生成物所具有的总能量,则反应是放热的,反之是吸热的,故A正确;
B、放热的反应在常温下不一定很容易发生,如:铝热反应2 Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe是放热反应,但需在高热条件下以保证足够的热量引发氧化铁和铝粉反应,故B错误;
C、中和热均为稀的强酸、强碱反应生成1mol水放出的热量,则两反应测定的中和热相等,故C正确;
D.符合燃烧热的概念,故D正确.
故选B.
点评 本题考查反应热的概念及燃烧热的定义,难度不大,注意放热反应在常温下不一定容易发生,如铝热反应.

练习册系列答案
相关题目
8.已知反应:①Cl2+2KBr=2KCl+Br2,②KClO3+6HCl=3Cl2↑+KCl+3H2O,③2KBrO3+Cl2=Br2+2KClO3,下列说法正确的是( )
| A. | 上述三个反应都有单质生成,所以都是置换反应 | |
| B. | 氧化性由强到弱顺序为Cl2>Br2>KBrO3>KClO3 | |
| C. | 反应②中还原剂与氧化剂的物质的量之比为5:1 | |
| D. | 反应③中1 mol KBrO3参加反应时有10 mol电子转移 |
5.过氧化钠可作为氧气的来源.常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 二氧化碳 | 碳酸钠 | 转移的电子 | |
| A | 1mol | NA | |
| B | 22.4L | 1mol | |
| C | 212g | 1mol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |
12.原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)X元素是H.
(2)X与W组成的化合物电子式为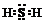 .
.
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O.
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下A 与NaOH溶液反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式:SO32-+Cl2+H2O=SO42-+2Cl-+2H+.
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶H2O.对化合物B进行如下实验:
2B的化学式为:(NH4)2SO4•FeSO4•6H2O.已知1mol/L 100mL B的溶液能与1mol/L 20mL KMnO4溶液(硫酸酸化)恰好反应.写出反应的离子方程式:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
(1)X元素是H.
(2)X与W组成的化合物电子式为
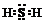 .
.(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O.
(4)由X、Y、Z、W四种元素组成的一种离子化合物A
①已知1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下A 与NaOH溶液反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
②又知A既能与盐酸反应,又能与氯水反应,写出A与氯水反应的离子方程式:SO32-+Cl2+H2O=SO42-+2Cl-+2H+.
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1mol B中含有6mol结晶H2O.对化合物B进行如下实验:
| 操作 | 现象 |
| ①取B的溶液加入过量浓 NaOH溶液并加热 | 产生白色沉淀和无色刺激性气味气体; 过一段时间白色沉淀变为灰绿色,最终变为红褐色; |
| ②另取B的溶液, 加入过量BaCl2溶液 | 产生白色沉淀,加盐酸沉淀不溶解 |
2.萜类物质中有许多都已被用于香料工业.常见的有如下几种结构(括号内表示④的结构简式),关于上述四种香料,下列说法正确的是( )
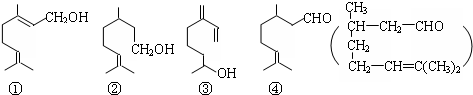

| A. | ④是②的氧化产物 | B. | ①③互为同系物 | ||
| C. | ②③均属于烯烃 | D. | ③④均能发生消去、酯化反应 |
9.常温下,下列溶液中微粒浓度关系一定正确的是( )
| A. | 氨水与氯化铵的pH=7的混合溶液中:c(Cl-)=c(NH4+) | |
| B. | 新制氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
 按要求写出下列化学方程式:
按要求写出下列化学方程式: .
.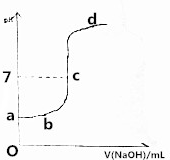 在研究弱电解质的电离、盐类的水解和溶液中离子浓度大小比较中,某师生共同做了这样一个实验:常温下,向20.0mL,0.1mol/LCH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,并在滴加过程中不断用pH计测量混合溶液的pH,绘出pH-V(NaOH)图象,如图所示.请分析:
在研究弱电解质的电离、盐类的水解和溶液中离子浓度大小比较中,某师生共同做了这样一个实验:常温下,向20.0mL,0.1mol/LCH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,并在滴加过程中不断用pH计测量混合溶液的pH,绘出pH-V(NaOH)图象,如图所示.请分析: