题目内容
2.化学实验操作是中学生必须掌握的实验技能,请按要求回答问题: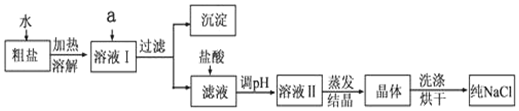
Ⅰ.粗盐除含NaCl外,还含有少量MgCl2、CaCl2、Na2SO4以及泥沙等杂质.如图所示是粗盐提纯的操作流程.提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、饱和NaCl溶液.
(1)除去溶液I中的MgCl2、CaCl2、Na2SO4,从提供的试剂中选出a所代表的试剂,按滴加顺序依次为:过量的NaOH溶液、过量的BaCl2溶液、过量的Na2CO3溶液;
(2)如何证明操作①中NaOH溶液已经过量?向上层清液中继续加入NaOH溶液,如果不产生白色沉淀则说明NaOH已经过量
(3)蒸发过程所用的主要仪器有:铁架台、酒精灯、蒸发皿、玻璃棒;
Ⅱ.某同学欲四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
(1)分离出四氯化碳层的操作是:将分液漏斗颈上的玻璃塞打开,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下并及时关闭活塞.
(2)分离碘的四氯化碳溶液的操作方法是:蒸馏.
分析 Ⅰ.(1)欲除去溶液中的MgCl2、CaCl2、Na2SO4,则用氢氧化钠除掉氯化镁,用氯化钡除掉硫酸钠,用碳酸钠除掉氯化钙与多余的氯化钡;
(2)氢氧化钠是沉淀镁离子的试剂,可以检验上层清液中是否含有镁离子,可以设计实验继续滴加氢氧化钠看是否生成白色沉淀;
(3)根据蒸发操作进行分析,蒸发溶液应在蒸发皿中进行;
Ⅱ.(1)四氯化碳萃取较高浓度的溴水中的溴利用的是分液,分液漏斗静置后放置在铁架台上,上层从上口倒出,下层从下口放出;
(2)碘被四氯化碳萃取溶解,分液后可以根据沸点不同通过蒸馏的方法分离得到溴单质.
解答 解:Ⅰ.(1)要除去溶液中的MgCl2、CaCl2、Na2SO4,所选试剂分别是氢氧化钠溶液,碳酸钠溶液和氯化钡溶液,根据题意要求,为了更好的把杂质除去,不带入新的杂质,所加溶液的顺序是氢氧化钠溶液,过量的BaCl2溶液,过量的Na2CO3溶液,
故答案为:过量的BaCl2溶液;过量的Na2CO3溶液;
(2)氢氧化钠是沉淀镁离子的试剂,可以检验上层清液中是否含有镁离子,可以设计实验继续滴加氢氧化钠看是否生成白色沉淀,步骤为:向上层清液中继续加入NaOH溶液,如果不产生白色沉淀则说明NaOH已过量,
故答案为:向上层清液中继续加入NaOH溶液,如果不产生白色沉淀则说明NaOH已经过量;
(3)蒸发溶液应在蒸发皿中进行,蒸发过程所用的主要仪器有:铁架台、酒精灯、蒸发皿、玻璃棒;
故答案为:蒸发皿;玻璃棒;
Ⅱ.(1)四氯化碳萃取较高浓度的溴水中的溴利用的是分液,分液漏斗静置后放置在铁架台上,上层从上口倒出,下层从下口放出;具体操作步骤为:将分液漏斗颈上的玻璃塞打开,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下并及时关闭活塞,
故答案为:将分液漏斗颈上的玻璃塞打开,再将分液漏斗下面的活塞拧开,使下层液体慢慢沿烧杯壁流下并及时关闭活塞;
(2);碘被四氯化碳萃取溶解,分液后可以根据沸点不同通过蒸馏的方法分离得到溴单质;
故答案为:蒸馏.
点评 本题考查粗盐提纯的操作,萃取,题目难度不大,注意除去食盐中的多种杂质,要根据除杂的原理,按照最优化的顺序添加除杂剂.

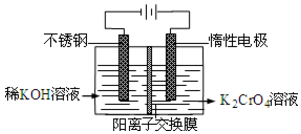 以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:下列说法不正确的是( )| A. | 在阴极式,发生的电极反应为:2H2O+2e-=2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程总反应的化学方程式为:4K2CrO4+4H2O$\frac{\underline{\;通电\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+2O2↑ | |
| D. | 测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=$\frac{d}{2}$ |
| A. | CuO+2H+═Cu2++H2O | B. | CaCO3+2H+═Ca2++CO2↑+H2O | ||
| C. | Fe+2H+═Fe2++H2↑ | D. | Ba(OH)2+2H+═Ba2++2H2O |
| A. | 加压 | B. | 加CuCl2固体 | C. | 加NaCl溶液 | D. | 加醋酸钠固体 |

| A. | 若A的分子式为C3H6O2,则其结构简式为CH3COOCH3 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子,且个数之比为1:2:3 | |
| C. | 仅由其核磁共振氢谱无法得知其分子中的氢原子总数 | |
| D. | 若A的化学式为C3H6O2,则其同分异构体有三种 |
| A. | 手持试管给试管内的物质加热 | |
| B. | 用燃着的酒精灯去点燃另一盏酒精灯 | |
| C. | 用天平称量药品时用手直接拿砝码 | |
| D. | 蒸馏操作时冷凝管中冷却水应该从下方通入,从上方流出 |
| A. | 第三周期有8种元素 | |
| B. | 短周期元素是指第一、二周期所含有的全部元素 | |
| C. | 元素周期表有8个主族 | |
| D. | IA族中的元素全部是金属元素 |



