题目内容
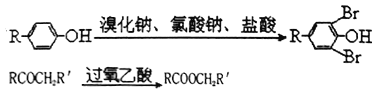
【题目】下列四种有机化合物的结构简式如下所示,均含有多个官能团,下列有关说法中正确的是( )

A. ①属于酚类,可与NaHCO3溶液反应产生CO2
B. ②属于酚类,能使FeCl3溶液显紫色
C. 1 mol ③最多能与3 mol Br2发生反应
D. ④属于醇类,可以发生消去反应
【答案】D
【解析】A、酚-OH不能与NaHCO3溶液反应,则A属于酚类,不与NaHCO3溶液反应产生CO2,选项A错误;B、②中不含酚-OH,所以不能使FeCl3溶液显紫色,选项B错误;C、酚-OH的邻、对位能与溴发生取代反应,所以1 molC最多能与2mol Br2发生反应,选项C错误;D、-OH与烃基相连,属于醇,且与-OH相连的C原子的邻位C原子上含H,能发生消去反应,选项D正确。答案选D。

练习册系列答案
相关题目