题目内容
下列实验操作中错误的是( )
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、向碘水中加入适量酒精,可以将碘单质萃取出来 |
| D、蒸发时,当溶液中出现大量晶体时,停止加热余热蒸干 |
考点:分液和萃取,蒸发和结晶、重结晶,蒸馏与分馏
专题:
分析:A.根据分液的操作目的判断;
B.根据蒸馏时,温度计测量的成分判断温度计的位置;
C.酒精和水互溶;
D.当蒸发皿中出现较多量的固体时即停止加热.
B.根据蒸馏时,温度计测量的成分判断温度计的位置;
C.酒精和水互溶;
D.当蒸发皿中出现较多量的固体时即停止加热.
解答:
解:A.分液时,为不产生杂质,分液漏斗下层液体从下口放出,上层液体从上口倒出,故A正确;
B.蒸馏时,温度计测量的是馏分的温度,所以温度计水银球应靠近蒸馏烧瓶支管口,故B正确;
C.酒精和水互溶,不能做萃取剂,故C错误;
D.蒸发结晶时应,当蒸发皿中出现较多量的固体时即停止加热,故D正确.
故选C.
B.蒸馏时,温度计测量的是馏分的温度,所以温度计水银球应靠近蒸馏烧瓶支管口,故B正确;
C.酒精和水互溶,不能做萃取剂,故C错误;
D.蒸发结晶时应,当蒸发皿中出现较多量的固体时即停止加热,故D正确.
故选C.
点评:本题考查了分液、蒸馏、蒸发结晶等实验操作,难度不大,实验是每年的必考题,要注重实验的学习、掌握.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O |
| B、过量的氨水滴加到氯化铝溶液中:Al3++4OH-═AlO2-+2H2O |
| C、次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
| D、Na2O2溶于水产生O2:2Na2O2+2H2O═4Na++4OH-+O2↑ |
根据下列化学实验事实得出的结论一定正确的是( )
| A、向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解.结论:该溶液中含有SO42- |
| B、向某无色溶液中加入足量盐酸,产生能使澄清石灰水变浑浊的气体.结论:该溶液中含有CO32-或HCO3- |
| C、向1 mL浓度均为0.05 mol/L的NaCl、NaI混合溶液中滴加2滴0.01 mol/L的AgNO3溶液,振荡,沉淀呈黄色.结论:Ksp(AgCl)<Ksp(AgI) |
| D、向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝.结论:该溶液中有NH4+ |
NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基准物质H2C2O4?2H2O的称量以及用NaOH溶液滴定等操作.下列有关说法正确的是( )
A、 用图所示操作转移NaOH溶液到容量瓶中 |
B、 用图所示装置准确称得0.1575gH2C2O4?2H2O固体 |
C、 用 用图所示操作排除碱式滴定管中的气泡 |
D、 用图所示装置以NaOH待测液滴定H2C2O4溶液 |
下列选项中的反应类型与其他三个选项反应类型不同的是( )
A、CH2=CH2+H2O
| ||
B、 +HNO3 +HNO3
 +H2O +H2O | ||
C、CH3COOH+CH3CH2OH
| ||
| D、CH3COOH+Cl2→ClCH2COOH+HCl |
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、滴入石蕊试液显蓝色的溶液中:K+、Na-、HSO3-、ClO- |
| B、0.1mol?L-l的Fe(NO3)2溶液中:Na+、H+、SCN-、I- |
| C、0.1mol?L-l的NaAlO2溶液中:K+、H+、NO3-、SO42- |
| D、由水电离产生的c(H+)=1×10-13mol?L-l的溶液中:Na+、Ba2+、NO3-、Cl- |
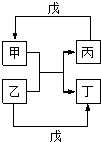 甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )
甲、乙、丙、丁、戊的相互转化关系如图(部分反应物及反应条件已略去,箭头表示一步转化).下列各组物质中,满足图示转化关系的是( )