题目内容
 (2013?江苏三模)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.
(2013?江苏三模)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标.(1)250℃时,以镍合金为催化剂,向4L容器中通入6mol CO2、6mol CH4,发生如下反应:CO2(g)+CH4(g)?2CO(g)+2H2(g).平衡体系中各组分体积分数如下表:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
64
64
.②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=2.8kJ?mol-1
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ?mol-1
反应CO2(g)+CH4(g)?2CO(g)+2H2(g) 的△H=
+247.3kJ?mol-1
+247.3kJ?mol-1
.(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.
①不同温度下催化剂的催化效率与乙酸的生成速率如右图所示.250~300℃时,温度升高而乙酸的生成速率降低的原因是
温度超过250℃时,催化剂的催化效率降低
温度超过250℃时,催化剂的催化效率降低
.②为了提高该反应中CH4的转化率,可以采取的措施是
增大反应压强或增大CO2的浓度
增大反应压强或增大CO2的浓度
.③将Cu2Al2O4溶解在稀硝酸中的离子方程式为
3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O
3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O
.(3)以CO2为原料可以合成多种物质.
①聚碳酸酯是一种易降解的新型合成材料,它是由加聚而成.写出聚碳酸酯的结构简式:
②以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为
CO2+8e-+6H2O=CH4+8OH-
CO2+8e-+6H2O=CH4+8OH-
.分析:(1)①先利用三段法求出各物质的物质的量,然后再根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积;
②根据盖斯定律来解答;
(2)①根据温度对催化剂活性的影响;
②根据外界条件对化学平衡的影响,平衡正向移动,反应物转化率增大;
③先将Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,再根据氧化物与酸反应生成离子方程式,需要注意的是一价铜具有还原性;
(3)以①根据加聚反应的特征来解答;
②根据原电池原理,CO2在正极发生还原反应转化为甲烷,注意电解质溶液为碱性.
②根据盖斯定律来解答;
(2)①根据温度对催化剂活性的影响;
②根据外界条件对化学平衡的影响,平衡正向移动,反应物转化率增大;
③先将Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,再根据氧化物与酸反应生成离子方程式,需要注意的是一价铜具有还原性;
(3)以①根据加聚反应的特征来解答;
②根据原电池原理,CO2在正极发生还原反应转化为甲烷,注意电解质溶液为碱性.
解答:解:(1)①CO2(g)+CH4(g)?2CO(g)+2H2(g).
起始(mol) 6 6 0 0
反应(mol) X X 2X 2X
平衡(mol) 6-X 6-X 2小 2X
由CH4的体积分数为0.1,则
=0.1,解得X=4,所以K=
=
=64,
故答案为:64;
②CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 ①
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=2.8kJ?mol-1 ②
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ?mol-1 ③
根据盖斯定律,由①+②×2-③×2得,CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=-890.3kJ?mol-1+2.8kJ?mol-1×2+566.0kJ?mol-1×2=+247.3 kJ?mol-1,
故答案为:+247.3 kJ?mol-1;
(2)①温度超过250℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低,故答案:温度超过250℃时,催化剂的催化效率降低;
②增大反应压强、增大CO2的浓度,平衡正向移动,反应物转化率增大,故答案为:增大反应压强、增大CO2的浓度;
③Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,与酸反应生成离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O,
故答案为:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
(3)①CO2发生加聚反应得到 ,故答案为:
,故答案为: ;
;
②CO2在正极发生还原反应转化为甲烷,电极反应为:CO2+8e-+6H2O=CH4+8OH-,故答案为:CO2+8e-+6H2O=CH4+8OH-.
起始(mol) 6 6 0 0
反应(mol) X X 2X 2X
平衡(mol) 6-X 6-X 2小 2X
由CH4的体积分数为0.1,则
| 6-X |
| 12+2X |
| C2(CO)C2(H2) |
| C (CO2)C(CH4) |
| 2 2×22 |
| 0.5×0.5 |
故答案为:64;
②CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ?mol-1 ①
CO(g)+H2O (g)=CO2(g)+H2 (g)△H=2.8kJ?mol-1 ②
2CO(g)+O2(g)=2CO2(g)△H=-566.0kJ?mol-1 ③
根据盖斯定律,由①+②×2-③×2得,CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=-890.3kJ?mol-1+2.8kJ?mol-1×2+566.0kJ?mol-1×2=+247.3 kJ?mol-1,
故答案为:+247.3 kJ?mol-1;
(2)①温度超过250℃时,催化剂的催化效率降低,所以温度升高而乙酸的生成速率降低,故答案:温度超过250℃时,催化剂的催化效率降低;
②增大反应压强、增大CO2的浓度,平衡正向移动,反应物转化率增大,故答案为:增大反应压强、增大CO2的浓度;
③Cu2Al2O4拆成氧化物的形式:Cu2O?Al2O3,与酸反应生成离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O,
故答案为:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
(3)①CO2发生加聚反应得到
②CO2在正极发生还原反应转化为甲烷,电极反应为:CO2+8e-+6H2O=CH4+8OH-,故答案为:CO2+8e-+6H2O=CH4+8OH-.
点评:本题主要考查了化学反应常数、化学平衡以及原电池原理的运用,难度不大,根据所学知识即可完成.

练习册系列答案
相关题目
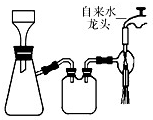 (2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下:
(2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下: