题目内容
(2013?江苏三模)常温下,下列各组离子在指定溶液中一定能大量共存的是( )
分析:A.离子之间不反应;
B.Cu2+为蓝色,且Cu2+、CO32-反应;
C.使pH试纸变红的溶液,显酸性;
D.水电离出的c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液.
B.Cu2+为蓝色,且Cu2+、CO32-反应;
C.使pH试纸变红的溶液,显酸性;
D.水电离出的c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液.
解答:解:A.离子之间不反应,则能共存,故A正确;
B.Cu2+为蓝色,与无色溶液不符,且Cu2+、CO32-反应,则不能共存,故B错误;
C.使pH试纸变红的溶液,显酸性,H+、ClO-结合生成弱酸,则不能共存,故C错误;
D.水电离出的c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液,碱溶液中NH4+、OH-结合生成弱电解质,则不能共存,故D错误;
故选A.
B.Cu2+为蓝色,与无色溶液不符,且Cu2+、CO32-反应,则不能共存,故B错误;
C.使pH试纸变红的溶液,显酸性,H+、ClO-结合生成弱酸,则不能共存,故C错误;
D.水电离出的c(H+)=10-12 mol?L-1的溶液,为酸或碱溶液,碱溶液中NH4+、OH-结合生成弱电解质,则不能共存,故D错误;
故选A.
点评:本题考查离子的共存,明确习题中的信息是解答本题的关键,选项C为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
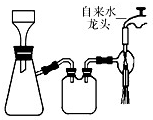 (2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下:
(2013?江苏三模)三草酸合铁(Ⅲ)酸钾晶体的化学式为K3[Fe(C2O4)3]?nH2O,常作为有机反应的催化剂.实验室可用(NH4)2Fe(SO4)2?2H2O等为原料制备,实验步骤如下: