题目内容
现往某单一溶质的溶液中加入NaOH溶液,开始时产生白色絮状沉淀,沉淀迅速变为灰绿色,最后变成红褐色,则该溶液中一定含有的阳离子为( )
| A、Fe3+ |
| B、Mg2+ |
| C、Fe2+ |
| D、Cu2+ |
考点:铁盐和亚铁盐的相互转变
专题:离子反应专题
分析:物质与氢氧化钠溶液反应,生成的白色絮状沉淀迅速变成灰绿色,是亚铁离子的特征性质和反应现象,据此分析判断;
解答:
解:物质与氢氧化钠溶液反应,生成的白色絮状沉淀迅速变成灰绿色,是亚铁离子的特征性质和反应现象,
反应为:Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故选C.
反应为:Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3.
故选C.
点评:本题考查了亚铁离子的性质分析和反应现象判断,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
下列有机物命名正确的是( )
A、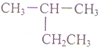 2-乙基甲烷 2-乙基甲烷 |
| B、CH3CH2CH2OH 1-丁醇 |
C、 对二甲苯 对二甲苯 |
D、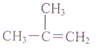 2-甲基-2-丙烯 2-甲基-2-丙烯 |
有一真空瓶质量为m1,该瓶充入空气后质量为m2.在相同状况下,若改为充入某气体A时,总质量为m3.则A的相对分子质量是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列各物质所含原子数目,按由多到少顺序排列的是( )
①11.2L NH3 ②标准状况下,4g He
③4℃时的9mL水 ④0.2mol H3PO4.
①11.2L NH3 ②标准状况下,4g He
③4℃时的9mL水 ④0.2mol H3PO4.
| A、①④③② | B、④③②① |
| C、②③④① | D、①④②③ |
1g氢气燃烧生成液态水放出142.9KJ热量,该反应的热化学方程式正确的是( )
| A、2H2(g)+O2(g)=2H2O( l )△H=-142.9 kJ?mol-1 |
| B、2H2(g)+O2(g)=2H2O( l )△H=-571.6 kJ?mol-1 |
| C、2H2+O2=2H2O△H=-571.6 kJ?mol-1 |
| D、2H2(g)+O2(g)=2H2O( l )△H=+571.6 kJ?mol-1 |
从碘水中提取碘,可供选择的有机试剂是( )
| A、苯、酒精 |
| B、汽油、甘油 |
| C、四氯化碳、直馏汽油 |
| D、二硫化碳、裂化汽油 |
下列说法正确的是( )
| A、自发反应一定是△H小于0的反应 |
| B、自发反应一定是△S大于0的反应 |
| C、丁达尔效应是区分胶体和溶液的一种常用物理方法 |
| D、硫酸钡不可能通过沉淀溶解平衡的移动转化为碳酸钡 |
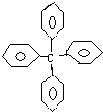 甲烷分子中的4个氢原子全部被苯基取代,可得分子的结构为,对该分子的叙述不正确的是( )
甲烷分子中的4个氢原子全部被苯基取代,可得分子的结构为,对该分子的叙述不正确的是( )| A、分子式为C25H20 |
| B、此物质不是苯的同系物 |
| C、此物质属于芳香烃 |
| D、该分子中所有原子有可能处于同一平面上 |