题目内容
12.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 1mol羟基中含有的电子数为10NA | |
| B. | 标准状况下,22.4 L CCl4含有的分子总数为NA | |
| C. | 46g组成为C2H6O的有机物,C-H键数目一定为5NA | |
| D. | 常温常压下,9g甲烷(14CH4)所含的中子数为4NA |
分析 A、羟基中含9个电子;
B、标况下四氯化碳为液态;
C、C2H6O可能为乙醇,也可能为二甲醚;
D、求出甲烷的物质的量,然后根据1mol甲烷中含8mol中子来分析.
解答 解:A、羟基中含9个电子,故1mol-OH中含9NA个电子,故A错误;
B、标况下四氯化碳为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故B错误;
C、C2H6O可能为乙醇,也可能为二甲醚,故46g此有机物即1mol中含有的C-H的个数可能为5NA个,也可能为6NA个,故C错误;
D、9g甲烷14CH4的物质的量b=$\frac{9g}{18g/mol}$=0.5mol,而1mol甲烷14CH4中含8mol中子,故0.5mol甲烷中含4NA个中子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
2.镁遇到下列物质不放出H2的是:( )
①NH4Cl溶液 ②KOH溶液 ③Na2CO3溶液 ④热的乙醇 ⑤苯
⑥醋酸溶液⑦FeCl3 溶液 ⑧CuSO4 溶液 ⑨NaH2PO4 ⑩NaHCO3 溶液.
①NH4Cl溶液 ②KOH溶液 ③Na2CO3溶液 ④热的乙醇 ⑤苯
⑥醋酸溶液⑦FeCl3 溶液 ⑧CuSO4 溶液 ⑨NaH2PO4 ⑩NaHCO3 溶液.
| A. | ①⑥⑦⑧ | B. | ③④⑤⑨⑩ | C. | ②③⑤⑩ | D. | ③④⑤⑦ |
3.下列有关甲烷物理性质的叙述正确的是( )
| A. | 甲烷是一种黄绿色气体 | |
| B. | 甲烷是一种有臭味的气体 | |
| C. | 收集甲烷时常用排水法,是因为甲烷的密度与空气的密度相近 | |
| D. | 甲烷能用排水法收集是因为甲烷难溶于水 |
20.被称为“国防金属”的镁,60%来自于海洋,从海水中提取镁的正确方法是( )
| 物质 | 氧化镁 | 氯化镁 |
| 熔点/℃ | 2 852 | 714 |
| A. | 海水$\stackrel{NaOH溶液}{→}$Mg(OH)2$\stackrel{通电}{→}$Mg | |
| B. | 海水$\stackrel{盐酸}{→}$MgCl2溶液-→MgCl2(熔融)$\stackrel{通电}{→}$Mg | |
| C. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{盐酸}{→}$MgCl2溶液-→MgCl2(熔融)$\stackrel{通电}{→}$Mg | |
| D. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{通电}{→}$Mg |
17.下列反应属于加成反应的是( )
| A. | 由乙烯与水反应制乙醇 | B. | 由甲烷制四氯化碳 | ||
| C. | 苯与浓硫酸、硝酸混合 | D. | 点燃乙醇 |
4.下列关于有机物的说法正确的是( )
| A. | 糖类、油脂、蛋白质都是高分子化合物 | |
| B. | 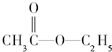 与 H$\stackrel{18}{2}$O发生水解反应,生成的产物中18O存在于乙醇中 与 H$\stackrel{18}{2}$O发生水解反应,生成的产物中18O存在于乙醇中 | |
| C. | 除去乙酸乙酯中混有的乙酸,可以加入乙醇继续酯化 | |
| D. | 油脂不管在哪种条件下水解都生成丙三醇(甘油) |
 .
.