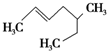
题目内容
如果将甲醇设计成燃料电池,其能量利用率会大幅度提高.甲醇和空气在氢氧化钠溶液中构成原电池,电池反应式为
2CH3OH+3O2+4NaOH═2Na2CO3+6H2O.在燃料电池中,甲醇在 (填“正极”或“负极”)充入并发生氧化反应.
2CH3OH+3O2+4NaOH═2Na2CO3+6H2O.在燃料电池中,甲醇在
考点:化学电源新型电池
专题:
分析:该燃料电池中,C元素化合价由-2价变为+4价,所以甲醇是还原剂,O元素化合价由0价变为-2价,所以氧气是氧化剂,还原剂在负极上失电子发生氧化反应,氧化剂在正极上得电子发生还原反应,据此分析解答.
解答:
解:该燃料电池中,C元素化合价由-2价变为+4价,O元素化合价由0价变为-2价,所以甲醇是还原剂、氧气是氧化剂,还原剂在负极上失电子发生氧化反应,氧化剂在正极上得电子发生还原反应,所以该燃料电池中,甲醇在负极上充入并发生氧化反应,故答案为:负极.
点评:本题以燃料电池为载体考查原电池原理,明确正负极上得失电子是解本题关键,根据元素化合价变化解答,易错点是判断甲醇中C元素化合价,题目难度不大.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
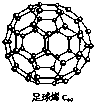 能源材料是当今科学研究的热点.氢气作为一种清洁能源,必须解决它的储存问题. C60(结构见图)可用作储氢材料.继C60后,科学家又合成了Si60、N60,它们的结构相似.下列有关说法正确的是( )
能源材料是当今科学研究的热点.氢气作为一种清洁能源,必须解决它的储存问题. C60(结构见图)可用作储氢材料.继C60后,科学家又合成了Si60、N60,它们的结构相似.下列有关说法正确的是( )| A、C60、Si60、N60都属于新型化合物 |
| B、C60、Si60、N60互为同分异构体 |
| C、N60结构中只存在N-N单键,而C60结构中既有C-C单键又有C=C双键 |
| D、已知金刚石中C-C键长154pm,C60中C-C键长140~145pm,故C60熔点高于金刚石 |
和水杨酸( )分子式相同,并且分子中含有6个碳原子在一条直线上,分子中所有官能团包括水杨酸具有的含氧官能团的有机物是( )
)分子式相同,并且分子中含有6个碳原子在一条直线上,分子中所有官能团包括水杨酸具有的含氧官能团的有机物是( )
 )分子式相同,并且分子中含有6个碳原子在一条直线上,分子中所有官能团包括水杨酸具有的含氧官能团的有机物是( )
)分子式相同,并且分子中含有6个碳原子在一条直线上,分子中所有官能团包括水杨酸具有的含氧官能团的有机物是( )| A、2种 | B、3种 | C、4种 | D、5种 |