题目内容
14.15g物质A和10.5g物质B完全反应,生成7.2g物质C、1.8g物质D和标准状况下6.72L的气态物质E,则物质E的摩尔质量是( )| A. | 16.5 g/mol | B. | 85 g/mol | C. | 55 g/mol | D. | 27.5 g/mol |
分析 依据质量守恒定律计算得出物质E的质量,然后利用n=$\frac{V}{{V}_{m}}=\frac{m}{M}$计算摩尔质量即可.
解答 解:根据质量守恒定律,得mE=15g+10.5g-7.2g-1.8g=16.5g,标准状况下6.72L的气态物质E的物质的量n=$\frac{V}{{V}_{m}}=\frac{m}{M}=\frac{6.72L}{22.4L/mol}$=0.3mol,所以E的摩尔质量=$\frac{m}{n}=\frac{16.5g}{0.3mol}$=55g/mol. 故选C.
点评 本题考查学生对教材公式的记忆情况以及质量守恒定律的应用,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
9.以下叙述中错误的是( )
| A. | 钠和氯气反应生成食盐后,其结构的稳定性增强 | |
| B. | 离子化合物不一定都易溶于水 | |
| C. | 任何离子键在形成的过程中必定有电子的得与失 | |
| D. | 钠和氧气反应生成过氧化钠后,体系的能量降低 |
5.可用于干燥NH3的试剂是( )
| A. | 无水CaCl2 | B. | 浓H2SO4 | C. | P2O5 | D. | 碱石灰 |
2.乙烯的产量是衡量一个国家石油化工生产水平的标志,这是由于乙烯在石油化工生产中具有广泛的用途.下列关于乙烯的用途叙述不正确的是( )
| A. | 以乙烯为原料可以合成聚乙烯等制备生活用品的材料 | |
| B. | 乙烯可以用来制备1,2-二氯乙烷(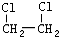 ) ) | |
| C. | 乙烯可以与水发生加成反应制备乙醇(CH3CH2OH) | |
| D. | 乙烯可以与Br2发生加成反应制备二溴乙烷(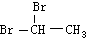 ) ) |
9.将质量相等的下列各物质完全酯化时,需醋酸质量最多的是( )
| A. | 甲醇 | B. | 乙二醇 | C. | 丙醇 | D. | 甘油 |
19.下列离子方程式错误的是( )
| A. | 硫酸与氢氧化钡反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2 H2O | |
| B. | 碳酸钙与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O | |
| C. | CO2通入过量的澄清石灰水中 CO2+Ca2++2OH-=CaCO3↓+H2O | |
| D. | 钠投入硫酸铜溶液中:2Na+Cu2+=2Na++Cu |
6.在实验室中,下列除去杂质的方法不正确的是( )
| A. | 硝基苯中混有NO2,加稀NaOH溶液反复洗涤、分液 | |
| B. | 乙烷中混有乙烯,将其通入溴水中洗气 | |
| C. | 获得无水乙醇的方法通常采用先用浓硫酸吸水,然后再加热蒸馏的方法 | |
| D. | 乙酸乙酯中混有乙酸,加饱和碳酸钠溶液反复洗涤、分液 |
3.下列实验可行的是( )
| A. | 用酸性高锰酸钾溶液除去乙烷中的乙烯 | |
| B. | 用苯与浓溴水在FeBr3催化作用下制溴苯 | |
| C. | 用食醋浸泡有水垢的水壶清除其中的水垢 | |
| D. | 用乙醇从碘水中萃取碘 |
4.下列关于说法中正确的是( )
| A. | CO(g)的燃烧热是283.0 kJ•mol-1,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0 kJ | |
| B. | H2SO4和NaOH反应的中和热△H=-57.3 kJ•mol-1,则1molH2SO4和1molBa(OH)2反应的反应热△H=-114.6kJ•mol-1 | |
| C. | 石墨转化为金刚石是吸热反应,可知金刚石的燃烧热更大 | |
| D. | 在恒温时,压缩容器的体积,则2SO2+O2?2SO3平衡正向移动,该反应的△H减小 |