题目内容
19.下列离子方程式错误的是( )| A. | 硫酸与氢氧化钡反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2 H2O | |
| B. | 碳酸钙与盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O | |
| C. | CO2通入过量的澄清石灰水中 CO2+Ca2++2OH-=CaCO3↓+H2O | |
| D. | 钠投入硫酸铜溶液中:2Na+Cu2+=2Na++Cu |
分析 A.反应生成硫酸钡和水,符合离子的配比;
B.反应生成氯化钙、水和二氧化碳,只有氯离子不参加反应;
C.反应生成碳酸钙和水;
D.反应生成氢氧化铜、氢气、硫酸钠.
解答 解:A.硫酸与氢氧化钡反应的离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A正确;
B.碳酸钙与盐酸反应的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,故B正确;
C.CO2通入过量的澄清石灰水中的离子反应为 CO2+Ca2++2OH-=CaCO3↓+H2O,故C正确;
D.钠投入硫酸铜溶液中的离子反应为2H2O+2Na+Cu2+=2Na++Cu(OH)2↓+H2↑,故D错误;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒分析,题目难度不大.

练习册系列答案
相关题目
10.氯化铜晶体(CuCl2•xH2O)是重要的化工原料,可用作催化剂、消毒剂等,用孔雀石[主要含Cu2(OH)2CO3,还含有少量Fe、Si的化合物]制备氯化铜晶体,方案如图:
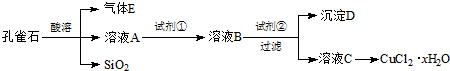
已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)酸溶时应选择酸的名称为盐酸;若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①可选用BE(填字母).
A.Cu B.Cl2 C.NH3•H2O D.NaOH E.H2O2 F.KMnO4
(2)加入试剂②的目的是调节pH至a,a的范围是3.7~5.4,写出试剂②的一种可能的化学式CuO、Cu(OH)2.由溶液C获得CuCl2•xH2O,包含4个基本实验操作,这4个基本实验操作依次是蒸发浓缩、冷却结晶、过滤、用无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是防止CuCl2•xH2O晶体溶解损失.
(3)为了测定制得的氯化铜晶体(CuCl2•xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是CuCl2•xH2O晶体加热时会发生水解.
②称取ag晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为bg.则x=$\frac{80a-135b}{18b}$(用含a、b的代数式表示).

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
| 离子种类 pH | Fe3+ | Cu2+ | Fe2+ |
| 开始沉淀 | 2.7 | 5.4 | 8.1 |
| 沉淀完全 | 3.7 | 6.9 | 9.6 |
A.Cu B.Cl2 C.NH3•H2O D.NaOH E.H2O2 F.KMnO4
(2)加入试剂②的目的是调节pH至a,a的范围是3.7~5.4,写出试剂②的一种可能的化学式CuO、Cu(OH)2.由溶液C获得CuCl2•xH2O,包含4个基本实验操作,这4个基本实验操作依次是蒸发浓缩、冷却结晶、过滤、用无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是防止CuCl2•xH2O晶体溶解损失.
(3)为了测定制得的氯化铜晶体(CuCl2•xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是CuCl2•xH2O晶体加热时会发生水解.
②称取ag晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为bg.则x=$\frac{80a-135b}{18b}$(用含a、b的代数式表示).
7.请用文字指出下图所示的装置和操作错在哪里,如何改正.
| 装 置 | NaOH溶液的存放 | 固体物质的称量 | 向容量瓶中转移溶液 |
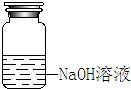 | 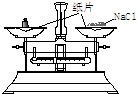 | 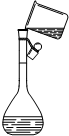 | |
| 错误之处 | 放在了带有磨口玻璃塞的广口瓶中 | 被称量的药品放在右边托盘 | 直接向容量瓶中转移溶液 |
| 如何改正 | 应放在带有橡胶塞的细口瓶中 | 应放在左边托盘中 | 应该用玻璃棒引流 |
14.15g物质A和10.5g物质B完全反应,生成7.2g物质C、1.8g物质D和标准状况下6.72L的气态物质E,则物质E的摩尔质量是( )
| A. | 16.5 g/mol | B. | 85 g/mol | C. | 55 g/mol | D. | 27.5 g/mol |
4.下列指定反应的离子方程式正确的是( )
| A. | 向漂白粉溶液中通入过量的SO2气体:ClO-+SO2+H2O═HSO3-+HClO | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 向Fe(NO3) 3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
11.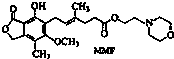 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
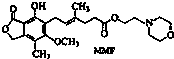 霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )
霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,结构简式如下.下列关于MMF说法中不正确的是( )| A. | MMF既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2反应发生取代 | |
| B. | 1molMMF能与含3molNaOH的水溶液完全反应 | |
| C. | MMF即可以催化加氢,又可以使酸性高锰酸钾溶液褪色 | |
| D. | MMF既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2 |
8.下列说法正确的是( )
| A. | 焓变是指1mol物质完全参加反应时的能量变化 | |
| B. | 中和滴定实验时,用待测液润洗锥形瓶 | |
| C. | 已知:2HI(g)?H2(g)+I2(g)△H=8.8kJ•mol-1,若向密闭容器中充入1molHI(g),则分解过程中吸收的热量为4.4kJ | |
| D. | 对于反应3H2(g)+N2(g)?2NH3(g),若使用催化剂,v正、v逆同等程度加快 |
9.下列物质与水反应,最终产物只有一种物质的是( )
| A. | 淀粉 | B. | 丙烯 | C. | 醋酸钠 | D. | 乙酸乙酯 |