题目内容
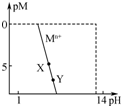 常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )
常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )| A、Mn+ 开始沉淀的pH与起始溶液c(Mn+)无关 |
| B、不同的金属沉淀完全时的pH相同 |
| C、图中Y点与X点pKsp相同 |
| D、Y点:pM=pKsp+npH-14n |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:Ksp=c(Mn+).cn(OH-),pKsp=-lgKsp=-lg(c(Mn+).cn(OH-))=-lg(c(Mn+).(
)n)=pKsp-npH+14n,以此解答该题.
| 10-14 |
| c(H+) |
解答:
解:A.Ksp=c(Mn+).cn(OH-),Mn+ 开始沉淀的pH与起始溶液c(Mn+)有关,故A错误;
B.不同的金属的Ksp不同,沉淀完全时的pH不同,故B错误;
C.Ksp只受温度的影响,温度不变,则Ksp不变,所以Y点与X点pKsp相同,故C正确;
D.pKsp=-lgKsp=-lg(c(Mn+).cn(OH-))=-lg(c(Mn+).(
)n)=pM-npH+14n,则pM=pKsp+npH-14n,故D正确.
故选CD.
B.不同的金属的Ksp不同,沉淀完全时的pH不同,故B错误;
C.Ksp只受温度的影响,温度不变,则Ksp不变,所以Y点与X点pKsp相同,故C正确;
D.pKsp=-lgKsp=-lg(c(Mn+).cn(OH-))=-lg(c(Mn+).(
| 10-14 |
| c(H+) |
故选CD.
点评:本题考查难溶电解质的溶解平衡,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,为解答该题的关键,难度中等.

练习册系列答案
相关题目
芳香化合物M的结构简式为 ,关于有机物M的说法正确的是( )
,关于有机物M的说法正确的是( )
 ,关于有机物M的说法正确的是( )
,关于有机物M的说法正确的是( )| A、有机物M的分子式为C10H12O3 |
| B、1mol Na2CO3最多能消耗1mol有机物M |
| C、1mol M和足量金属钠反应生成22.4L气体 |
| D、有机物M能发生取代、氧化、还原和加聚反应 |
在周期表中,第2、4、6周期元素的数目分别是( )
| A、8、8、18 |
| B、8、18、18 |
| C、8、8、32 |
| D、8、18、32 |
污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀.下列物质不能作为沉淀剂的是( )
| A、氨水 | B、硫化氢气体 |
| C、硫酸钠溶液 | D、纯碱溶液 |
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
| C、化合物YW2、ZW2都是酸性氧化物 |
| D、用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是( )
| A、有色布条被空气中的氧气氧化 |
| B、漂白粉溶液失去了部分水分,浓度增大了 |
| C、漂白粉和空气中的二氧化碳充分反应生成了次氯酸 |
| D、漂白粉被氧化了 |
做下列有机实验时,操作正确的是( )
| A、检验某溶液中是否含有甲醛:在盛有2mL 10%硫酸铜溶液的试管中滴加10%的氢氧化钠溶液0.5mL,混合均匀,滴入待检液后煮沸 |
| B、实验室制取硝基苯:先加入苯,再加浓硫酸,最后滴入浓硝酸 |
| C、制取溴苯:将铁屑、溴水和苯混合后共热 |
| D、提取溶解在水中的碘:加入CCl4振荡、静置、分层后取出有机层再分离 |
下列装置中能构成原电池的是( )
A、 |
B、 |
C、 |
D、 |