题目内容
在周期表中,第2、4、6周期元素的数目分别是( )
| A、8、8、18 |
| B、8、18、18 |
| C、8、8、32 |
| D、8、18、32 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:在周期表中,第2、4、6周期元素的数目分别是8、18、32,据此分析解答.
解答:
解:在周期表中,第二周期只含主族和0族,所以一共含有8种元素;
第四周期中包含7个主族、7个副族、1个0族、一个第VIII族,第VIII族含有3种元素,所以第四周期一共有18种元素;
第六周期中包含7个主族、7个副族、1个0族、一个第VIII族,第VIII族含有3种元素,第IIIB族镧系含有15种元素,所以一共含有32种元素,
故选D.
第四周期中包含7个主族、7个副族、1个0族、一个第VIII族,第VIII族含有3种元素,所以第四周期一共有18种元素;
第六周期中包含7个主族、7个副族、1个0族、一个第VIII族,第VIII族含有3种元素,第IIIB族镧系含有15种元素,所以一共含有32种元素,
故选D.
点评:本题考查了元素周期表结构及其应用,明确元素周期表结构及每一周期元素种类数是解本题关键,注意第VIII族和镧系、锕系中元素种类数,为易错点.

练习册系列答案
相关题目
关于氢键,下列说法中,正确的是( )
| A、氢键比范德华力强,所以它属于化学键 |
| B、分子间形成的氢键使物质的熔点和沸点升高 |
| C、含氢原子的物质之间均可形成氢键 |
| D、H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列化合物中,含有非极性共价键的离子化合物是( )
| A、CaC2 |
| B、N2H4 |
| C、Na2S2 |
| D、NH4NO3 |
下列叙述不正确的是( )
| A、根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量 |
| B、CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液 |
| C、根据金属活动性顺序表,可以推断冶炼金属时可能的方法 |
| D、根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行 |
NaCl是一种化工原料,可以制备一系列物质(如图所示).下列说法正确的是( )
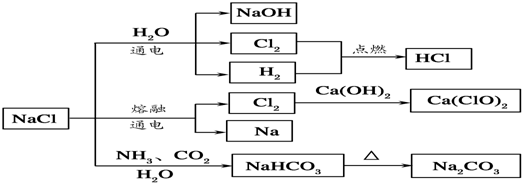

| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B、石灰乳和Cl2反应可制得漂白粉,其主要成分是次氯酸钙 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、如图所示转化反应不都是氧化还原反应 |
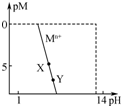 常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )
常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )| A、Mn+ 开始沉淀的pH与起始溶液c(Mn+)无关 |
| B、不同的金属沉淀完全时的pH相同 |
| C、图中Y点与X点pKsp相同 |
| D、Y点:pM=pKsp+npH-14n |
某硫酸厂废气中SO2的回收利用方案如图所示.下列说法不正确的是( )


| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y可能含有(NH4)2SO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
下列离子方程式的书写符合前提所述的情况的是( )
| A、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-→NH3↑+H2O |
| B、在NH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:Al3++2SO42-+2Ba2++4OH-→2BaSO4↓+AlO2-+2H2O |
| C、当Ba(OH)2和NaHSO4 混合恰好呈中性:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O |
| D、向烧碱溶液中通入CO2,当n(NaOH):n(CO2)=3:2时:OH-+CO2→HCO3- |