题目内容
7.已知下列化合物:①FeCl2②Na2CO3③Al(OH)3④Na2O2⑤NaHCO3⑥Fe(OH)3,其中能通过化合反应制取的有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
分析 ①FCl3与Fe反应生成FeCl2属于化合反应;
②氧化钠和二氧化碳反应可生成碳酸钠;
③氧化铝和水不反应;
④氧气和钠在加热条件下可生成过氧化钠;
⑤Na2CO3和二氧化碳、水反应生成NaHCO3;
⑥氢氧化亚铁和氧气、水反应生成氢氧化铁,以此解答.
解答 解:①FCl3与Fe反应能生成FeCl2,其方程式为:2FCl3+Fe=3FeCl2,属于化合反应;
②氧化钠和二氧化碳反应可生成碳酸钠,属于化合反应;
③氧化铝和水不反应,不能通过化合反应生成;
④钠与氧气在加热的条件下生成Na2O2发生化合反应;
⑤Na2CO3和二氧化碳、水反应生成NaHCO3,Na2CO3+H2O+CO2=2NaHCO3,属于化合反应;
⑥氢氧化亚铁和氧气、水反应生成氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3,属于化合反应.
故选C.
点评 本题综合考查了元素化合物知识、化学反应类型等,为高频考点,侧重于双基的考查,难度不大,掌握元素化合物的知识是关键.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
18.下列有关氯碱工业的描述,正确的是( )
| A. | 氯碱工业是指电解熔融氯化钠制取氯气的方法 | |
| B. | 氯碱工业只能得到氯气和氢氧化钠两种有价值的产品 | |
| C. | 实验室模拟氯碱工业制取氯气后所得溶液呈碱性 | |
| D. | 实验室模拟氯碱工业所得氯气不能直接排放,应用澄清石灰水吸收 |
15.难溶电解质的溶解平衡属于动态平衡.已知几种难溶电解质的溶度积(25℃时,忽略溶液混合时的体积变化)如下表.
(1)常温下,将适量Li2CO3固体溶于水配成Li2CO3悬浊液,该悬浊液中c(Li+)=0.12mol•L-1,则c(CO32-)=
0.06mol/L
(2)一定温度下,将0.1molAgCl加入1L0.1mol•L-1Na2CO3溶液中,充分搅拌,写出该反应的离子方程式:2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)溶液中$\frac{c(C{{O}^{2-}}_{3})}{{c}^{2}(C{l}^{-})}$为2.5×10-8
(3)常温下,向5ml含有KCl和KI浓度均为0.01mol•L-1的溶液中加入8mL0.01mol•L-1AgNO3溶液,此时溶液中溶质的离子浓度大小关系为c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-).
| 化学式 | AgCl | Ag2CO3 | AgI | Li2CO3 |
| 溶度积(K甲 ) | 2×10-10 | 1×10-11 | 8.5×10-17 | 8.64×10-4 |
0.06mol/L
(2)一定温度下,将0.1molAgCl加入1L0.1mol•L-1Na2CO3溶液中,充分搅拌,写出该反应的离子方程式:2AgCl(s)+CO32-(aq)?Ag2CO3(s)+2Cl-(aq)溶液中$\frac{c(C{{O}^{2-}}_{3})}{{c}^{2}(C{l}^{-})}$为2.5×10-8
(3)常温下,向5ml含有KCl和KI浓度均为0.01mol•L-1的溶液中加入8mL0.01mol•L-1AgNO3溶液,此时溶液中溶质的离子浓度大小关系为c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-).
2.已知a、b、d、e分别是Cu、Ag、Fe、Mg五种金属中的一种,实验测得其分别具有以下性质:①a能与稀硫酸反应放出气体;②b与d的硝酸盐反应,置换出单质d;③e的最高价阳离子遇KSCN溶液显血红色.由此判断a、b、d、e分别是( )
| A. | Fe、Cu、Ag、Mg | B. | Cu、Mg、Ag、Fe | C. | Mg、Cu、Ag、Fe | D. | Mg、Ag、Cu、Fe |
4.在容积为2L的密闭容器中进行反应,CO(g)+2H2(g)?CH3OH(g),其他条件不变,在300℃和500℃时,n(CH3OH)与反应时间t的变化曲线如图,下列说法正确的是( )


| A. | 该反应的△H<0 | |
| B. | 其他条件不变,升高温度反应的平衡常数增大 | |
| C. | 300℃时,0~t1min内CH3OH的平均生成速率为$\frac{{n}_{1}}{{t}_{1}}$1mol•L-1•min-1 | |
| D. | A点的反应体系温度从300℃升高到500℃,达到平衡时,$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$减小 |
8.下列叙述中,正确的是( )
| A. | 同温同压下,等体积的气体所含有的原子数相同 | |
| B. | 在氧化还原反应中金属单质作反应物时定做还原剂 | |
| C. | 发生离了反应,生成物要同时具备有难溶物、难电离物质和挥发性物质 | |
| D. | 盐酸中逐滴加入Na2CO3溶液和Na2CO3溶液中逐滴加入盐酸现象完全一样 |
9.还原剂被氧化后得到的产物称为氧化产物,氧化剂被还原后得到的产物为还原产物.关于反应:3(NH4)2SO4$\frac{\underline{\;强热\;}}{\;}$3SO2↑+N2↑+4NH3↑+6H2O的说法正确的是( )
| A. | SO2为还原产物,NH3为氧化产物 | |
| B. | 所得三种气体形成的混合气体平均摩尔质量可能为16 g/mol | |
| C. | 被氧化的氮元素与未被氧化的氮元素质量比为1:2 | |
| D. | 相同条件下,产生的三种气体原子数之比为3:1:4 |
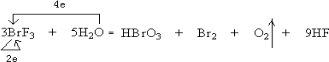 ,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)
,还原剂是H2O和BrF3,氧化剂是BrF3.氧化产物是HBrO3、O2. 还原产物是Br2(以上均填化学式)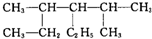 其名称是2,4-二甲基-3-乙基-己烷.
其名称是2,4-二甲基-3-乙基-己烷.