题目内容
19.第3周期某主族元素的原子,在同周期中它的第一电离能仅大于Na,下列关于此元素的叙述正确的是( )| A. | 该元素的单质能在CO2中燃烧 | |
| B. | 该元素的氢氧化物具有两性 | |
| C. | 该元素的原子半径比钠的原子半径大 | |
| D. | 1mol该元素的单质可与酸反应产生1molH2 |
分析 同周期元素从左到右第一电离能呈逐渐增大趋势,但ⅡA族最外层电子为全充满结构,较为稳定,大于ⅢA族第一点电离能,则第3周期某主族元素的原子,第一电离能顺序为Na<Al<Mg<Si<…在同周期中它的第一电离能仅大于Na,应为Al元素,以此解答该题.
解答 解:由以上分析可知该元素为Al,
A.铝与二氧化碳不反应,故A错误;
B.氢氧化铝为两性氢氧化物,故B正确;
C.同周期元素从左到右原子半径逐渐减小,故C错误;
D.1mol铝与酸反应,生成铝离子,化合价为+3价,失去3mol电子,则生成1.5mol氢气,故D错误.
故选B.
点评 本题考查原子结构与元素周期率,为高频考点和常见题型,侧重考查学生的分析能力,注意把握同周期元素的性质的递变规律,难度不大.

练习册系列答案
相关题目
9.下列说法中一定正确的是( )
| A. | pH=5的溶液中c(H+)=1.0×10-5 mol•L-1 | |
| B. | pH=7的溶液呈中性 | |
| C. | pH值为0的溶液中c(H+)=0 mol/L | |
| D. | pH=5的溶液中c(OH-)=1.0×10-9 mol•L-1 |
10.下列物质在水溶液中的电离方程式错误的是( )
| A. | (NH4)2SO4=2NH4++SO42- | B. | NaHS?Na++HS${\;}^{_}$,HS-=H++S2- | ||
| C. | Ba(OH)2=Ba2++2OH- | D. | HF?H++F- |
4.室温下,分别用0.1mol•L-1溶液进行下列实验,结论不正确的是( )
| A. | 向NaOH溶液中通SO2至pH=7:c(Na+)═c(HSO3-)+2c(SO32-) | |
| B. | 向NH4Cl溶液中加入等浓度等体积的NH3•H2O后,所得溶液呈碱性,则:c(NH4+)<c(NH3•H2O) | |
| C. | 向NH4HSO4加入等浓度等体积的NaOH溶液后后:c(NH4+)+c(NH3•H2O)═c(Na+) | |
| D. | 向CH3COOH溶液中加入少量CH3COONa晶体:$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ 增大 |
11.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| B | C2H5OH与浓硫酸170℃共热,制得的气体通入酸性KMnO4溶液 | KMnO4溶液褪色 | 使KMnO4溶液褪色的气体一定是乙烯 |
| C | 铜放入稀硫酸中,再加入硝酸钠固体 | 开始无明显现象,后溶液变蓝,有气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向浓度均为0.1mol/L NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
8.化学与生产、生活、社会密切相关.下列说法正确的是( )
| A. | 误服BaCl2中毒,可服用硫酸钠溶液解毒 | |
| B. | PM2.5颗粒(直径约为2.5×10-6m)分散到空气中形成气溶胶 | |
| C. | 硅可用于制造光电池和高性能的现代通讯材料 | |
| D. | 汽车尾气中含有的氮氧化物是汽油不完全燃烧生成的 |
2.下列物质的分类正确的是( )
| 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | CaF2 | CO | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO2 |
| A. | A | B. | B | C. | C | D. | D |
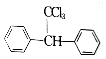 ,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为2:2:2:1.
,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为2:2:2:1.