题目内容
有原子序数依次相差1,且由小到大排列的A、B、C、D、E五种短周期元素,下列是有关这五种元素的叙述:
①若A的最高价氧化物的水化物是强碱,则E的最高价氧化物的水化物一定是强酸
②若A的单质既能与强酸反应又能与强碱反应且都放出氢气,则这五种元素在同一周期
③若A的阳离子比E的阴离子少8个电子,则D一定是非金属元素
④若D的最高价氧化物的水化物是强酸,则E的单质在常温下为气态
其中正确的是
- A.①②③
- B.②③④
- C.①③④
- D.①②④
B
当五种元素位于第二周期时①结论成立,位于第三周期时①结论不成立,如:A为Na,则E为P;A单质既能与强酸又能与强碱反应,则A为铝元素,故五种元素位于同一周期,②正确;A的阳离子比E的阴离子少8个电子,则A和E位于同一周期,二、三周期中D一定为非金属,③正确;D的最高价氧化物的水化物是强酸,故D为S,E为Cl,故④正确。
当五种元素位于第二周期时①结论成立,位于第三周期时①结论不成立,如:A为Na,则E为P;A单质既能与强酸又能与强碱反应,则A为铝元素,故五种元素位于同一周期,②正确;A的阳离子比E的阴离子少8个电子,则A和E位于同一周期,二、三周期中D一定为非金属,③正确;D的最高价氧化物的水化物是强酸,故D为S,E为Cl,故④正确。

练习册系列答案
相关题目
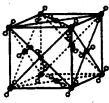 短周期元素E、F的离子F+与E2-核外电子排布相同,B、D、E元素的原子序数依次递增,B原子的每个能级上电子数相等,BE2和D2E是等电子体、A是F所在周期非金属性最强的元素,G.E同主族且原子核外电子层数相差两层,
短周期元素E、F的离子F+与E2-核外电子排布相同,B、D、E元素的原子序数依次递增,B原子的每个能级上电子数相等,BE2和D2E是等电子体、A是F所在周期非金属性最强的元素,G.E同主族且原子核外电子层数相差两层, A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的原子半径最 小;B元素的最高价氧化物对应水化物与其氢化物能生成盐;D与A同主族,且与E同周 期;E元素原子的最外层电子数是其次外层电子数的