题目内容
向溴水中加入足量乙醛溶液,可以看到溴水褪色。据此对溴水与乙醛发生的有机反应类型进行如下探究,请你完成下列填空:
I.猜测:
(1)溴水与乙醛发生取代反应;
(2)溴水与乙醛发生加成反应;
(3)溴水与乙醛发生_______反应。
II.设计方案并论证:
为探究哪一种猜测正确,某研究性学习小组提出了如下两种实验方案:
方案l:检验褪色后溶液的酸碱性。
方案2:测定反应前用于溴水制备的Br2的物质的量和反应后Br-离子的物质的量。
(1)方案1是否可行? _______,理由是__________________________________________
(2)假设测得反应前用于溴水制备的Br2的物质的量为a mol 。
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生加成反应;;
若测得反应后n(Br-) = _______mol,则说明溴水与乙醛发生取代反应;
若测得反应后n(Br-) = _______mol,则说明猜测(3)正确。
III.实验验证:某同学在含0.005molBr2的10mL溶液中,加入足量乙醛溶液使其褪色;再加入过量AgNO3溶液,得到淡黄色沉淀l.88 g(已知反应生成有机物与AgNO3不反应)。根据计算结果,推知溴水与乙醛反应的离子方程式为__________________________________________。
IV.拓展
请你设计对照实验,探究乙醛和乙醇的还原性强弱(填写下表)。
| 实验操作步骤 | 实验现象 | 结论 |
| | | |
I.(3)氧化(1分)
II.(1)不可行(1分) 溴水与乙醛发生取代反应和乙醛被溴水氧化都有HBr生成,溶液均呈酸性(2分)
(2)0 (1分) a (1分) 2a(1分)
III.CH3CHO+Br2+H2O=CH3COOH+2H++2Br-(2分)
IV.实验操作步骤 实验现象 结论 在两支洁净的试管中分别加入2mL新制银氨溶液(或新制氢氧化铜),各滴入3滴(或0.5mL)乙醛和乙醇振荡,水浴加热(或加热)试管(3分) 滴入乙醛的试管中有银镜(或红色沉淀)生成,而滴入乙醇的试管中无现象(1分) 乙醛的还原性比乙醇强(1分)
解析试题分析:
I.根据溴水的性质和乙醛的结构片断去推两者可能的反应是取代、加成或氧化;
II.(1)显然是不可行的,因为无论是溴水与乙醛发生的是取代反应还氧化反应产物中都有HBr生成,溶液均会呈现出酸性;
(2)根据加成、取代、氧化反应的特点可知n(Br-)分别为0、a、2a;
III.经过计算AgBr的物质的量为0.01mol,整好是Br2的2倍,因而发生的是氧化反应。
V.设计实验探究乙醛和乙醇的还原性强弱,可以利用醛基的强还原性可以和银氨溶液或新制Cu(OH)2悬浊液的反应来进行验证。
考点:本题以探究实验为基础,考查了溴水和乙醛反应的实质、探究实验的基本方法、有机反应的特点以及化学实验的基础知识。

铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药品,下表是说明书的部分内容。
[规格]每片含琥珀酸亚铁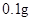 [适应症]用于缺铁性贫血症,预防及治疗用。 [用量用法]成人预防量 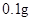 /日,成人治疗量 /日,成人治疗量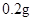 — —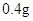 /日。 /日。小儿用量预防量 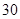 — —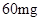 /日,治疗量 /日,治疗量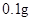 — —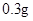 /日 /日[贮藏]避光、密封、在干燥处保存。 |
(1)该药品中Fe2+会缓慢氧化。国家规定该药物中Fe2+的氧化率(已经被氧化Fe2+的质量与Fe2+总质量的比值)超过10.00% 即不能再服用。
①实验室可采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+进行滴定(假设药品中其他成份不与KMnO4反应)。请写出该反应的离子方程式: 。
②实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的玻璃仪器除玻璃棒、烧杯、胶头滴管外,还需 。
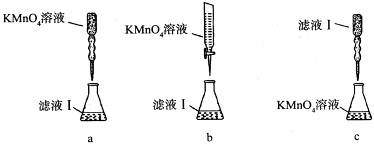
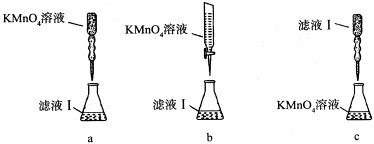
③某同学设计了下列滴定方式(夹持部分略去),最合理的是 。(填字母序号)
(2)称量上述含铁元素质量分数为20.00%的“速力菲”10.00 g,将其全部溶于稀H2SO4中,配制成1000 ml溶液,取出20.00 ml,用0.01000 mol?L-1的KMnO4溶液滴定,用去KMnO4溶液12.00 ml ,该药品中Fe2+的氧化率为 。
(3)已知琥珀酸为二元有机羧酸,含23.6 g琥珀酸的溶液与4.0 mol?L-1 100.0 ml的氢氧化钠溶液恰好完全中和。核磁共振氢谱分析显示,琥珀酸分子谱图上只有两组吸收峰。写出琥珀酸溶液与氢氧化钠溶液完全中和的化学方程式(有机物写结构简式) 。
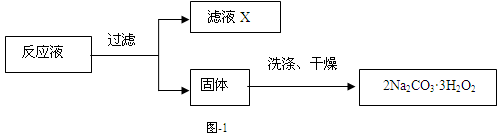
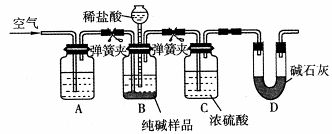
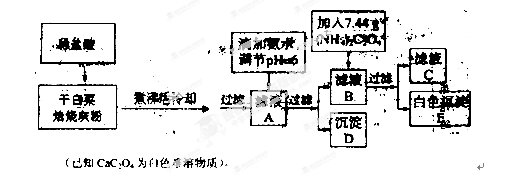
白云石的主要成分为CaCO3、MgCO3,还含有少量Fe、Si的化合物,实验室以白云石为原料制Mg(OH)2及CaCO3。步骤如下:
实验过程中需要的数据见下表:
| | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Mg2+ | 9.5 | 11.0 |
请回答下列问题:
(1)过滤中所需的玻璃仪器是 。溶液A中含有Ca2+,Mg2+,Fe2+,Fe3+,则试剂①可选择
(填字母)
A.KMnO4 B.Cl2 C.H2O2
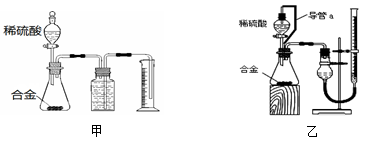
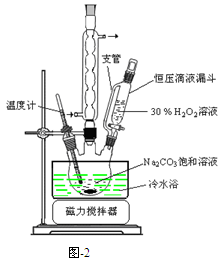
(2)若要利用反应过程中生成的CO2,从溶液D中制取CaCO3,需要先通入的一种气体是 ,然后通入CO2。通入CO2气体时请把右边的装置图补充完整(不允许更换溶液,导气管以下连接的仪器自选)。
(3)根据表中提供的数据判断,Fe(OH)3、Fe(OH)2和Mg(OH)2的溶度积常数由小到大的排列顺序为 。

(4)若将制取的Mg(OH)2:加入到某聚乙烯树脂中,树脂可燃性大大降低,Mg(OH)起阻燃作用的主要原因是 。
现有三组溶液:①汽油和氯化钠溶液;②39%的乙醇溶液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是 ( )
| A.分液、萃取、蒸馏 | B.分液、蒸馏、萃取 |
| C.萃取、蒸馏、分液 | D.蒸馏、萃取、分液 |
小华家中有如下生活用品:碘酒、食盐、食醋、84消毒液(内含NaClO),小华利用上述用品不能完成的任务是
| A.检验买来的奶粉中是否加有淀粉 | B.检验自来水中是否含有Cl- |
| C.除去保温瓶中的水垢 | D.洗去白色衣服上的番茄汁 |