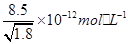题目内容
在平衡体系Ca(OH)2(s) 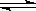 Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
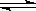 Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是
Ca2+ +2OH一中,能使c(Ca2+)减小,而使c(OH一)增大的是| A.加入少量MgCl2固体 | B.加入少量Na2CO3固体 |
| C.加入少量KCl固体 | D.加入少量Ba(OH)2固体 |
BD
试题分析:Ca(OH)2(s)
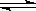 Ca2+ +2OH一中,加入少量MgCl2固体,能使c(Ca2+)增大,而使c(OH一)减小,故A错误;加入少量Na2CO3固体,能使c(Ca2+)减小,而使c(OH一)增大,故B正确;加入少量KCl固体 ,溶液中c(Ca2+),c(OH一)不变,平衡不移动,故C错误;加入少量Ba(OH)2固体,c(Ca2+)减小,虽然平衡向左移动,但是根据勒夏特勒原理可以知道,c(OH一)比原来还是大了,所以D也正确,故本题的答案选择BD。
Ca2+ +2OH一中,加入少量MgCl2固体,能使c(Ca2+)增大,而使c(OH一)减小,故A错误;加入少量Na2CO3固体,能使c(Ca2+)减小,而使c(OH一)增大,故B正确;加入少量KCl固体 ,溶液中c(Ca2+),c(OH一)不变,平衡不移动,故C错误;加入少量Ba(OH)2固体,c(Ca2+)减小,虽然平衡向左移动,但是根据勒夏特勒原理可以知道,c(OH一)比原来还是大了,所以D也正确,故本题的答案选择BD。点评:本题考查了难溶电解质的溶解平衡,该考点是高考考查的重点和热点,本题D选择比较容易漏选,要根据勒夏特勒原理来判断。该题难度中等。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____:
Fe+2NaCl,该电池放电时,正极反应式为 ________________ _____: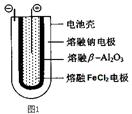
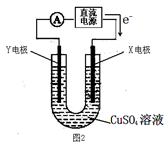
 HCO3-+OH-,下列说法正确的是( )
HCO3-+OH-,下列说法正确的是( ) 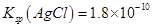 ,
, 。下列关于不溶物之间转化的说法中错误的是:
。下列关于不溶物之间转化的说法中错误的是: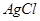 不溶于水,不能转化为
不溶于水,不能转化为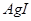
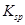 相差越大,不溶物就越容易转化为更难溶的不溶物
相差越大,不溶物就越容易转化为更难溶的不溶物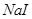 溶液中开始转化为
溶液中开始转化为