��Ŀ����
��ʽ̼��ͭ��һ����;�㷺�Ļ���ԭ�ϡ���ҵ�Ͽ������Կ�ʴ��Һ����Ҫ�ɷ���Cu2+��Fe2+��Fe3+��H +��Cl-���Ʊ������Ʊ��������£�

Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
��1�������Ƶ������� ����������Ҫ�ɷ��� ��д��ѧʽ����
��2�����ڷ�ӦA����Һ��pH��ΧӦΪ ������ѡ����Լ��� ������ţ���
a����ˮ b��ϡ���� c���������� d��̼��ͭ
��3����ӦB���¶�����ߣ�����������ɫ��Ʒ�п��ܻ���ֵ������� ����д��ѧʽ��
��4�����˵õ��IJ�Ʒϴ��ʱ������жϲ�Ʒ�Ѿ�ϴ���� ��
��5����Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ�������
�� ������ֻ��CuCO3������Ӧ�����ӷ���ʽΪ ��
�� ������ֻ��Cu(OH)2������Ӧ�����ӷ���ʽ��ʾ����� ��
�� ������Cu(OH)2��CuCO3�Ļ�������ʽ�Σ�����˵�� ��
��6����ʽ̼��ͭ��ɿɱ�ʾΪ��aCuCO3?bCu(OH)2?cH2O����ͨ�����з����ⶨ����ɡ��������£�
�� ������Ʒ���� ���·ֽ⣻�� ���CO2���������� ���ˮ�������������� ����CuO��
��������ⶨ�����������ۡ� ��

Cu2+��Fe2+��Fe3+���ɳ�����pH���£�
| ���� | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| ��ʼ����pH | 4.2 | 5.8 | 1.2 |
| ��ȫ����pH | 6.7 | 8.3 | 3.2 |
��1�������Ƶ������� ����������Ҫ�ɷ��� ��д��ѧʽ����
��2�����ڷ�ӦA����Һ��pH��ΧӦΪ ������ѡ����Լ��� ������ţ���
a����ˮ b��ϡ���� c���������� d��̼��ͭ
��3����ӦB���¶�����ߣ�����������ɫ��Ʒ�п��ܻ���ֵ������� ����д��ѧʽ��
��4�����˵õ��IJ�Ʒϴ��ʱ������жϲ�Ʒ�Ѿ�ϴ���� ��
��5����Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ�������
�� ������ֻ��CuCO3������Ӧ�����ӷ���ʽΪ ��
�� ������ֻ��Cu(OH)2������Ӧ�����ӷ���ʽ��ʾ����� ��
�� ������Cu(OH)2��CuCO3�Ļ�������ʽ�Σ�����˵�� ��
��6����ʽ̼��ͭ��ɿɱ�ʾΪ��aCuCO3?bCu(OH)2?cH2O����ͨ�����з����ⶨ����ɡ��������£�
�� ������Ʒ���� ���·ֽ⣻�� ���CO2���������� ���ˮ�������������� ����CuO��
��������ⶨ�����������ۡ� ��
��1����Fe2+������Fe3+�����ճ�ȥ��1�֣���Fe(OH)3��1�֣�����2��3.2-4.2��1�֣���d��1�֣�����3��CuO��1�֣�����4��ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ�������������Ҳ���֣�1�֣�����5����Cu2++CO32-��CuCO3����1�֣���
��CO32-+H2O
 OH��+HCO3-��Cu2++2OH����Cu(OH)2����2�֣���
OH��+HCO3-��Cu2++2OH����Cu(OH)2����2�֣�����̼��ͭ��������ͭ���ܽ���������1�֣���6��ʵ��ֻ��ⶨ�ĸ����е��������ɡ���2�֣�
�����������1�������Ƶ������ǽ�Fe2+������Fe3+�����ճ�ȥ����������Ҫ�ɷ���Fe(OH)3����2�����ڷ�ӦA����Һ��pH��ΧӦΪ3.2-4.2������ѡ����Լ���̼��ͭ���Ҳ������µ����ʡ���3����ӦB���¶�����ߣ���ʽ̼��ͭ���ܻ���ֵ�����������ͭ����4��ȡ���һ��ϴ��Һ��������������ϡ���ᣬ���������������ϴ�Ӹɾ�����5����Na2CO3��Һ���뵽һ����CuCl2��Һ�еõ��������� ������ֻ��CuCO3������Ӧ�����ӷ���ʽΪCu2++CO32-=CuCO3������ ������ֻ��Cu(OH)2������Ӧ�����ӷ���ʽ��ʾ�����CO32-+H2O
 OH��+HCO3-��Cu2++2OH����Cu(OH)2������ ������Cu(OH)2��CuCO3�Ļ�������ʽ�Σ�����˵��̼��ͭ��������ͭ���ܽ�����������6����ʽ̼��ͭ��ɿɱ�ʾΪ��aCuCO3?bCu(OH)2?cH2O����ͨ�����з����ⶨ����ɡ��������£��� ������Ʒ���� ���·ֽ⣻�� ���CO2���������� ���ˮ�������������� ����CuO��ʵ��ֻ��ⶨ�ĸ����е��������ɡ���
OH��+HCO3-��Cu2++2OH����Cu(OH)2������ ������Cu(OH)2��CuCO3�Ļ�������ʽ�Σ�����˵��̼��ͭ��������ͭ���ܽ�����������6����ʽ̼��ͭ��ɿɱ�ʾΪ��aCuCO3?bCu(OH)2?cH2O����ͨ�����з����ⶨ����ɡ��������£��� ������Ʒ���� ���·ֽ⣻�� ���CO2���������� ���ˮ�������������� ����CuO��ʵ��ֻ��ⶨ�ĸ����е��������ɡ���
��ϰ��ϵ�д�
 һ���㶨ϵ�д�
һ���㶨ϵ�д� ��У��ҵ��ϵ�д�
��У��ҵ��ϵ�д� ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
�����Ŀ
 Ba2��(aq)��SO42-(aq)��Ksp��c(Ba2��)��c(SO42-)�������ܽ�ƽ��������ͼ��ʾ������˵����ȷ����
Ba2��(aq)��SO42-(aq)��Ksp��c(Ba2��)��c(SO42-)�������ܽ�ƽ��������ͼ��ʾ������˵����ȷ����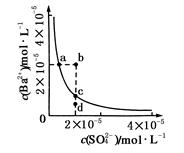
 Pb2��(aq)��2I��(aq)�����ټ�������PbI2���壬����˵������ȷ����
Pb2��(aq)��2I��(aq)�����ټ�������PbI2���壬����˵������ȷ����  Ag����aq����Cl����aq��������AgCl�ֱ���� ��100mLˮ�У���50mL0.1mol/L NaCl��Һ�У���10mL0.1mol/LAgNO3��Һ�У���20mL0.1mol/L MgCl2��Һ�С����������ͬ���¶���Ag��Ũ���ɴ�С��˳���ǣ�
Ag����aq����Cl����aq��������AgCl�ֱ���� ��100mLˮ�У���50mL0.1mol/L NaCl��Һ�У���10mL0.1mol/LAgNO3��Һ�У���20mL0.1mol/L MgCl2��Һ�С����������ͬ���¶���Ag��Ũ���ɴ�С��˳���ǣ�

 10-20�����¶��·�Ӧ��Cu2����2H2O
10-20�����¶��·�Ӧ��Cu2����2H2O Cu(OH)2��2H����ƽ�ⳣ��K= ��
Cu(OH)2��2H����ƽ�ⳣ��K= �� FexNy��H2 (δ��ƽ��,���������������İ���34.0g�����ij�����ʯ2kg������������������ģ���FexNy�ŷ۵Ļ�ѧʽΪ ��
FexNy��H2 (δ��ƽ��,���������������İ���34.0g�����ij�����ʯ2kg������������������ģ���FexNy�ŷ۵Ļ�ѧʽΪ �� Ca2+ +2OHһ�У���ʹc(Ca2+)��С����ʹc(OHһ)�������
Ca2+ +2OHһ�У���ʹc(Ca2+)��С����ʹc(OHһ)�������