题目内容
向100mL pH=0的硫酸和硝酸混合溶液中投入3.84g铜粉,微热使反应充分完成后,生成NO气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
| A.0.02mol | B.0.08mol | C.0.10mol | D.0.16mol |
A
解析试题分析:溶液中氢离子的物质的量是0.1mol,NO的物质的量是0.02mol,转移0.02mol×3=0.06mol电子。而铜的物质的量是0.06mol,如果完全反应,则转移0.12mol电子。所以根据反应式3Cu+8H++2NO3-=3Cu2++4H2O+2NO↑可知,氢离子是过量的,所以硝酸不足,完全反应,即反应前硝酸的物质的量就是0.02mol,答案选A。
考点:考查硝酸和金属的有关计算
点评:该题的根据是进行过量计算。由于在酸性条件下,硝酸盐也具有氧化性,所以该题在判断过量问题时,应该用离子方程式进行,如果用化学方程式则会得出错误的结论。

练习册系列答案
相关题目
(7分)
(1)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得如下数据:
|
序号 |
Ba(OH)2溶液的体积/mL |
盐酸的体积/mL |
溶液的pH |
|
① |
22.00 |
0.00 |
12 |
|
② |
22.00 |
18.00 |
11 |
|
③ |
22.00 |
22.00 |
7 |
x = ____________ ;Ba(OH)2溶液的物质的量浓度为____
(2)常温下,向100mL pH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH ______7(填“>”“<” 或“=”);原混合溶液中硫酸钠的物质的量浓度为
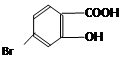 ,它的含氧官能团名称为 、 。
,它的含氧官能团名称为 、 。