题目内容
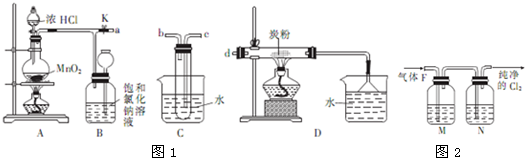
 如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1mol X分解得到A、B、C各1mol.
如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X和H是固体,B和G是液体,其余均为气体,1mol X分解得到A、B、C各1mol.试回答下列各题:
(1)写出下列物质的化学式:X
(2)写出下列反应的化学方程式:
①H+G-→A+F:
②C+D-→E:
(3)写出下列反应的离子方程式:
G+Cu-→E:
考点:无机物的推断
专题:
分析:常温下X和H是固体,B和G是液体,其余均为气体由框图可知X既能与酸反应生成气体A,又能与碱反应生成气体C,故X应为弱酸的铵盐,该弱酸易分解,而且产生的气体能与Na2O2反应,猜想X应为NH4HCO3或(NH4)2CO3,又知1 mol X分解得到A、B、C各1 mol,故X只能是NH4HCO3,A为CO2,B为H2O,C为NH3,D为O2,E为NO,F为NO2,G为HNO3,H为C,结合对应物质的性质以及题目要求可解答该题.
解答:
解:常温下X和H是固体,B和G是液体,由框图可知X既能与酸反应生成气体A,又能与碱反应生成气体C,故X应为弱酸的铵盐,该弱酸易分解,而且产生的气体能与Na2O2反应,猜想X应为NH4HCO3或(NH4)2CO3,又知1 mol X分解得到A、B、C各1 mol,故X只能是NH4HCO3,A为CO2,B为H2O,C为NH3,D为O2,E为NO,F为NO2,G为HNO3,H为C,
(1)由以上分析可知X为NH4HCO3,B为H2O,故答案为:NH4HCO3;H2O;
(2)①H+G→A+F为C和浓硝酸的反应,方程式为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O;
②C+D→E的反应为4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
(3)铜和稀硝酸反应生成硝酸铜和一氧化氮,反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
(1)由以上分析可知X为NH4HCO3,B为H2O,故答案为:NH4HCO3;H2O;
(2)①H+G→A+F为C和浓硝酸的反应,方程式为C+4HNO3(浓)
| ||
故答案为:C+4HNO3(浓)
| ||
②C+D→E的反应为4NH3+5O2
| ||
| △ |
| ||
| △ |
(3)铜和稀硝酸反应生成硝酸铜和一氧化氮,反应的离子方程式为3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
故答案为:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O;
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和推断能力的考查,注重于元素化合物知识的综合运用,化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合.它不仅可考查学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法.解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
CuO和Fe2O3的混合物m g,向其中加入1mol?L-1的HNO3溶液200mL恰好完全反应,若将2m g该混合物用足量CO还原,充分反应后剩余固体质量为( )
| A、3.2 g |
| B、(2m-3.2)g |
| C、(m-1.6)g |
| D、(2m-1.6)g |
恒温恒容条件下,存在可逆反应:aA(g)?bB(g),当反应处于平衡状态时,下列说法中不正确的是( )
| A、无论a、b大小关系如何,再加入气体A时,平衡一定向正反应方向移动 |
| B、若a<b,再加入A并达到平衡时,A的体积分数较原平衡更大 |
| C、若a>b,再加入A时,A的转化率增大 |
| D、加入气体A后,当反应再次达到平衡时,反应速率与原平衡时的反应速率相等 |
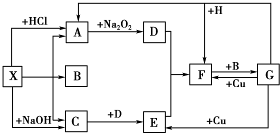
某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( )
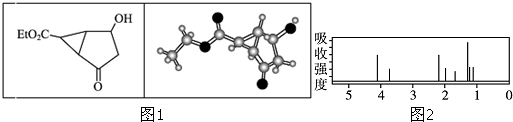

| A、该有机物不同化学环境的氢原子有6种 |
| B、该有机物属于芳香化合物 |
| C、键线式中的Et代表的基团为-CH3 |
| D、该有机物在一定条件下能够发生消去反应 |
下列说法正确的是( )
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下一定很易发生 |
| C、热化学方程式中的计量数可表示分子的个数 |
| D、吸热反应在一定的条件下也能自发进行 |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)=c(NH4+) |
| B、两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1<10c2 |
| C、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液呈酸性 |
D、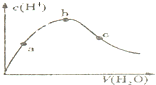 向冰醋酸中逐渐加水,有如图变化.a、b、c三点中水的电离程度最大的是b点 |
在2SO2+O2=2SO3(正反应放热)的平衡体系中,下列条件可使反应速率加快,且平衡向右移动的是( )
| A、升高温度 |
| B、增加压强 |
| C、减小SO3的浓度 |
| D、使用催化剂 |
常用一些图案标示危险化学品的类别.化学物质与其上方的标示图案相符的( )
A、 氮气 |
B、 金属钠 |
C、 浓盐酸 |
D、 浓硫酸 |