题目内容
火力发电厂释放出的大量NOx、SO2、CO2会对环境造成污染.对燃煤废气进行脱硝、脱硫和脱碳处理,可实现节能减排、废物利用等目的.
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1
甲烷直接将NO2还原为N2的热化学方程式为 .
(2)脱碳.CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H3
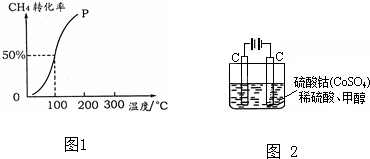
①将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应.反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1,则上述CO2转化为甲醇的反应的△H3 0(填“>”、“<”或“=”).
②图2是用于笔记本电脑的甲醇燃料电池结构示意图,质子交换膜左右两侧的溶液均为1L 2mol/L H2SO4溶液,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为 (忽略气体的溶解,假设反应物完全耗尽).

(3)脱硫.①某种脱硫工艺中将废气处理后,与一定量的氨气、空气、水反应,生成硫酸铵和硝酸铵的混合物作为副产品氮肥.设废气中SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为 .
②25℃时pH均为4的硝酸铵溶液和稀硝酸中由水电离出的氢离子浓度分别为c1、c2,则c1与c2的比值等于 .
(1)脱硝.利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1
甲烷直接将NO2还原为N2的热化学方程式为
(2)脱碳.CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H3
①将CO2和H2的混合气体分成五等份,将它们分别充入温度不同、容积相同的恒容容器中发生上述反应.反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1,则上述CO2转化为甲醇的反应的△H3
②图2是用于笔记本电脑的甲醇燃料电池结构示意图,质子交换膜左右两侧的溶液均为1L 2mol/L H2SO4溶液,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为

(3)脱硫.①某种脱硫工艺中将废气处理后,与一定量的氨气、空气、水反应,生成硫酸铵和硝酸铵的混合物作为副产品氮肥.设废气中SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为
②25℃时pH均为4的硝酸铵溶液和稀硝酸中由水电离出的氢离子浓度分别为c1、c2,则c1与c2的比值等于
考点:用盖斯定律进行有关反应热的计算,化学电源新型电池
专题:化学反应中的能量变化,电化学专题
分析:(1)根据盖斯定律,利用已知化学反应方程式乘以某个系数相加或相减,构造出目标化学反应方程式,该化学反应的焓变即为已知化学反应方程式的焓变乘以某个系数相加或相减得到;
(2)①由图可知,到达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行;
②负极反应式为CH3OH-6e-+H2O=CO2+6H+,正极反应式为O2+4H++4e-=2H2O,按照电极反应式计算;
(3)①根据反应物和生成物结合守恒的方法书写化学方程式;
②硝酸铵水解促进水的电离,C1=10-4 mol/L,稀醋酸抑制水的电离,C2=c(OH-)=
=10-10 mol/L.
(2)①由图可知,到达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行;
②负极反应式为CH3OH-6e-+H2O=CO2+6H+,正极反应式为O2+4H++4e-=2H2O,按照电极反应式计算;
(3)①根据反应物和生成物结合守恒的方法书写化学方程式;
②硝酸铵水解促进水的电离,C1=10-4 mol/L,稀醋酸抑制水的电离,C2=c(OH-)=
| 10-14 |
| 10-4 |
解答:
解:(1)已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ?mol-1,
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1,
不管化学反应是一步完成还是分几步完成,其反应热是相同的.利用盖斯定律将两式相加,可得
2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol,
即CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ?mol-1,
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ/mol;
(2)①由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H3<0,故答案为:<;
②负极反应式为CH3OH-6e-+H2O=CO2+6H+,当转移1mol电子时,左侧质量减轻
×12g=2g,还要有1molH+通过质子交换膜进入右侧,质量减少1g,正极反应式为O2+4H++4e-=2H2O,右侧质量增加32g×
=8g,加上转移过来的1gH+,因此左右两侧溶液的质量之差为8g+1g+2g+1g=12g,
故答案为:12;
(3)①烟气中的SO2、NO2的物质的量之比为1:1,一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.则有12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3,
故答案为:12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3;
②硝酸铵水解促进水的电离,C1=10-4 mol/L,稀醋酸抑制水的电离,C2=c(OH-)=
=10-10 mol/L,因此则c1与c2的比值等于
=106,
故答案为:106 .
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ?mol-1,
不管化学反应是一步完成还是分几步完成,其反应热是相同的.利用盖斯定律将两式相加,可得
2CH4(g)+4NO2(g)=2N2(g)+2CO2(g)+4H2O(g)△H=-1734 kJ/mol,
即CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ?mol-1,
故答案为:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ/mol;
(2)①由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H3<0,故答案为:<;
②负极反应式为CH3OH-6e-+H2O=CO2+6H+,当转移1mol电子时,左侧质量减轻
| 1 |
| 6 |
| 1 |
| 4 |
故答案为:12;
(3)①烟气中的SO2、NO2的物质的量之比为1:1,一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.则有12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3,
故答案为:12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3;
②硝酸铵水解促进水的电离,C1=10-4 mol/L,稀醋酸抑制水的电离,C2=c(OH-)=
| 10-14 |
| 10-4 |
| 10-4 |
| 10-10 |
故答案为:106 .
点评:本题考查较为综合,涉及化学平衡的计算、化学平衡的移动以及电化学知识,综合考查学生的分析能力和计算能力,把握电极方程式的书写,注意质子交换膜的性质,难度中等.

练习册系列答案
相关题目
下列正确的是( )
| A、将一定量氨气通入0.1 mol?L-1 NH4Cl溶液中可能有:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、AgCl沉淀易转化成AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)>K(AgCl) |
| C、F、Cl、Br、I的非金属性逐渐减弱,HF、HCl、HBr、HI水溶液的酸性逐渐减弱 |
| D、短周期元素形成离子后,最外层均达8电子稳定结构 |
在测定中和热的实验中,使用下列用品不是为了减小实验误差的是( )
| A、碎泡沫塑料 | B、环形玻璃棒 |
| C、硬纸板 | D、两个量筒 |
在一定容积为2L的恒温恒容容器中,加入1molN2和4molH2,5分钟达到平衡,测得平衡时容器内压强是开始的0.92倍,计算用H2表示的反应速率 ;N2的转化率为 ;平衡混合气体中H2的百分含量 .