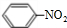题目内容
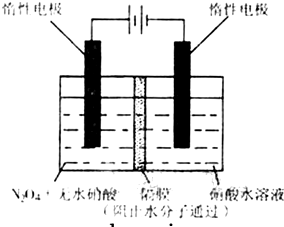
已知 ,如图所示装置可用来制取
,如图所示装置可用来制取 并比较S元素与Br元素非金属性的强弱.
并比较S元素与Br元素非金属性的强弱.

(1)将下列操作步骤补充完整:
①______________________________________________________________________________
②用大火加热使S粉沸腾与 化合;
化合;
③______________________________________________________________________________
④停止加热并做善后处理.
(2)Ⅰ中制 不直接用稀
不直接用稀 与Zn反应;而将浓
与Zn反应;而将浓 滴入水中,其优点是________.
滴入水中,其优点是________.
(3)Ⅲ中发生的现象是________,得出的结论是________.
解析:
|
(1)连接好装置、检测装置气密性、滴入浓 (2)稀释浓 (3)有黄色沉淀生成,Br的非金属性比S强 |

 名校课堂系列答案
名校课堂系列答案(分)纯碱、烧碱等是重要的化工原料。
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 。若其它操作不变,将A与C连接,可观察到的现象是 。

(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3 g白色固体,该白色固体的组成是 (写化学式)。
设计实验确认该白色固体中存在的阴离子,试完成下列方案。
| 实验操作 | 实验现象 | 结论 | |
| ① 取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | |||
| ② 过滤,取2 mL滤液于试管中 | |||
| ③ | |||
(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知NaHCO3在低温下溶解度较小。反应I为:
NaCl+CO2+NH3+H2O![]() NaHCO3↓+NH4Cl,处理母液的两种方法如下。
NaHCO3↓+NH4Cl,处理母液的两种方法如下。
① 向母液中加入石灰乳,可将其中 循环利用,同时得到融雪剂 。
② 向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:_______________________________________。
(11分)纯碱、烧碱等是重要的化工原料。
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是 。若其它操作不变,将A与C连接,可观察到的现象是 。
(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3 g白色固体,该白色固体的组成是 (写化学式)。
设计实验确认该白色固体中存在的阴离子,试完成下列方案。
| 实验操作 | 实验现象 | 结论 | |
| ① 取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 |
|
| |
| ② 过滤,取2 mL滤液于试管中 | |||
| ③ |
|
| |
(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知NaHCO3在低温下溶解度较小。反应I为:
NaCl+CO2+NH3+H2ONaHCO3↓+NH4Cl,处理母液的两种方法如下。
① 向母液中加入石灰乳,可将其中 循环利用,同时得到融雪剂 。
② 向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:_______________________________________。
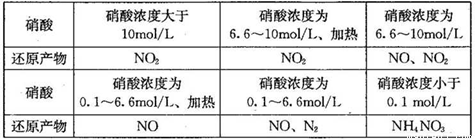
 ,将导管插入
,将导管插入 水中,并控制反应
水中,并控制反应 ,放热使反应加快
,放热使反应加快