题目内容
为测定某有机化合物A的结构,进行如下实验.
【分子式的确定】
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下).则该物质的实验式是 ;
(2)质谱仪测定有机物A的相对分子质量为46,则该物质的分子式是 ;
(3)预测A的可能结构并写出结构简式 、 .
【结构式的确定】
(4)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(图1甲).经测定,有机物A的核磁共振氢谱图如图1乙,则A的结构简式为 .

【性质实验】
某实验小组用图2装置进行A的催化氧化的实验.
(5)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式: 、 在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇的氧化反应是 反应.
(6)甲和乙两个水浴作用不相同.甲的作用是 ;乙的作用是
(7)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有 .要除去该物质,可先在混合液中加入 (填写字母).a.氯化钠溶液 b.苯c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填实验操作名称)即可除去.
【分子式的确定】
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下).则该物质的实验式是
(2)质谱仪测定有机物A的相对分子质量为46,则该物质的分子式是
(3)预测A的可能结构并写出结构简式
【结构式的确定】
(4)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(图1甲).经测定,有机物A的核磁共振氢谱图如图1乙,则A的结构简式为

【性质实验】
某实验小组用图2装置进行A的催化氧化的实验.
(5)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学反应方程式:
(6)甲和乙两个水浴作用不相同.甲的作用是
(7)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
然后,再通过
考点:测定有机物分子的元素组成
专题:
分析:(1)n(CO2)=
=0.2mol,n(H2O)=
=0.3mol,n(O2)=
=0.3mol,结合质量守恒定律推断;
(2)质谱仪测定有机化合物的相对分子质量为46,结合最简式判断分子式为C2H6O;
(3)A可能为乙醇或二甲醚;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,二甲醚只有一种不同化学环境的氢原子;
(5)乙醇在铜做催化剂条件被氧气氧化成乙醛,属于加氧的氧化反应,方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,熄灭酒精灯,反应仍能继续进行,说明该反应是放热反应;
(6)依据乙醇和乙醛的物理性质:二者都容易挥发.乙醇是反应物,应转化成乙醇蒸汽进入到硬质试管内参与反应;乙醛是产物,降低温度使其转化成液态,所以前者用热水浴,后者用冷水浴;
(7)乙醛能被氧气氧化为乙酸,酸性物质能使紫色石蕊试纸显红色;根据乙酸的化学性质进行解答;分离相互溶解的液体,可以利用蒸馏法.
| 8.8g |
| 44g/mol |
| 5.4g |
| 18g/mol |
| 6.72L |
| 22.4L/mol |
(2)质谱仪测定有机化合物的相对分子质量为46,结合最简式判断分子式为C2H6O;
(3)A可能为乙醇或二甲醚;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,二甲醚只有一种不同化学环境的氢原子;
(5)乙醇在铜做催化剂条件被氧气氧化成乙醛,属于加氧的氧化反应,方程式为:2CH3CH2OH+O2
| Cu |
| △ |
(6)依据乙醇和乙醛的物理性质:二者都容易挥发.乙醇是反应物,应转化成乙醇蒸汽进入到硬质试管内参与反应;乙醛是产物,降低温度使其转化成液态,所以前者用热水浴,后者用冷水浴;
(7)乙醛能被氧气氧化为乙酸,酸性物质能使紫色石蕊试纸显红色;根据乙酸的化学性质进行解答;分离相互溶解的液体,可以利用蒸馏法.
解答:
解:(1)n(CO2)=
=0.2mol,n(H2O)=
=0.3mol,n(O2)=
=0.3mol,则有机物中含n(O)=0.2mol×2+0.3mol-0.6mol=0.1mol,则有机物中N(C):N(H):N(O)=0.2mol:0.6mol:0.1mol=2:6:1,故有机物A的实验式为C2H6O,
故答案为:C2H6O;
(2)实验式为C2H6O,有机化合物的相对分子质量为46,实验式即为分子式,则该物质的分子式是C2H6O,故答案为:C2H6O;
(3)A可能为乙醇或二甲醚,结构简式为CH3CH2OH、CH3-O-CH3,故答案为:CH3CH2OH、CH3-O-CH3;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即CH3CH2OH,二甲醚只有一种不同化学环境的氢原子,故答案为:CH3CH2OH;
(5)铜丝变黑是因为发生反应:2Cu+O2
2CuO,后来变红是因为发生反应:CH3CH2OH+CuO
CH3CHO+Cu+H2O,该反应是乙醇的催化氧化,铜在反应中做催化剂;
熄灭酒精灯,反应仍能继续进行,说明该反应时一个放热反应,
故答案为:2Cu+O2
2CuO;CH3CH2OH+CuO
CH3CHO+Cu+H2O;放热;
(6)根据反应流程可知:在甲处用热水浴加热使乙醇挥发与空气中的氧气混合,有利于下一步反应;乙处作用为冷水浴,降低温度,使生成的乙醛冷凝成为液体,沉在试管的底部,
故答案为:加热;冷却;
(7)乙醛能被进一步氧化成乙酸,乙酸能使紫色石蕊试纸显红色,所以若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中含有乙酸;四个选择中,只有“c.碳酸氢钠”可以和乙酸反应,生成乙酸钠、水和二氧化碳,所以c正确;将两种互溶物质分离,通常采用蒸馏法,
故答案为:乙酸;c;蒸馏.
| 8.8g |
| 44g/mol |
| 5.4g |
| 18g/mol |
| 6.72L |
| 22.4L/mol |
故答案为:C2H6O;
(2)实验式为C2H6O,有机化合物的相对分子质量为46,实验式即为分子式,则该物质的分子式是C2H6O,故答案为:C2H6O;
(3)A可能为乙醇或二甲醚,结构简式为CH3CH2OH、CH3-O-CH3,故答案为:CH3CH2OH、CH3-O-CH3;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即CH3CH2OH,二甲醚只有一种不同化学环境的氢原子,故答案为:CH3CH2OH;
(5)铜丝变黑是因为发生反应:2Cu+O2
| ||
| Cu |
| △ |
熄灭酒精灯,反应仍能继续进行,说明该反应时一个放热反应,
故答案为:2Cu+O2
| ||
| Cu |
| △ |
(6)根据反应流程可知:在甲处用热水浴加热使乙醇挥发与空气中的氧气混合,有利于下一步反应;乙处作用为冷水浴,降低温度,使生成的乙醛冷凝成为液体,沉在试管的底部,
故答案为:加热;冷却;
(7)乙醛能被进一步氧化成乙酸,乙酸能使紫色石蕊试纸显红色,所以若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中含有乙酸;四个选择中,只有“c.碳酸氢钠”可以和乙酸反应,生成乙酸钠、水和二氧化碳,所以c正确;将两种互溶物质分离,通常采用蒸馏法,
故答案为:乙酸;c;蒸馏.
点评:本题考查有机物的推断,化学实验基本操作以及乙醇的催化氧化实验等方面的知识,属于综合知识的考查,综合性较强,题目难度中等,注意掌握乙醇的催化反应原理,能够正确书写反应的化学方程式,试题有利于培养学生的分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温条件下,下列各组离子在指定溶液中能大量共存的是( )
| A、使石蕊试液变红的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B、由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO3-、K+ |
| C、c(H+)/c(OH-)=1×1012的溶液中:NH4+、Cl-、SO42-、Al3+ |
| D、c(Al3+)=0.1 mol/L的溶液中:K+、Cl-、SO42-、CO32- |
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2 与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、铜与稀硝酸反应:Cu+4H++2NO3-═2H2O+Cu2++2NO2↑ | ||||
| C、足量氨水吸收少量二氧化硫气体:NH3?H2O+SO2=NH4++HSO3- | ||||
| D、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
下列物质中,在一定条件下既能发生银镜反应,又能发生水解和氧化反应的是( )
| A、乙酸甲酯 | B、溴乙烯 |
| C、甲酸乙酯 | D、苯甲醛 |
实验是研究化学的基础,图中所示的实验方法、装置或操作完全正确的是( )
A、 饱和食盐水 |
B、 稀释 |
C、 制气 |
D、 称量 |
某同学用下列装置制备并检验Cl2的性质.下列说法错误的是( )
A、 即使MnO2过量,盐酸也不能全部消耗 |
B、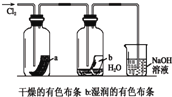 湿润的有色布条能褪色 |
C、 生成棕色的烟 |
D、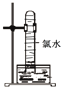 用光照射氯水后液体颜色加深 |
 为了研究CaCO3与稀盐酸反应的反应速率,某学生将少量CaCO3颗粒加入到500mL浓度为 2.0mol/L的稀盐酸中,通过实验测定:在标准状况下放出气体的物质的量(标准状况下)和时间的关系如右图所示.请依图回答下列问题:
为了研究CaCO3与稀盐酸反应的反应速率,某学生将少量CaCO3颗粒加入到500mL浓度为 2.0mol/L的稀盐酸中,通过实验测定:在标准状况下放出气体的物质的量(标准状况下)和时间的关系如右图所示.请依图回答下列问题: