题目内容
 (1)如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面人低于b端液面的是
(1)如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体 ②浓硫酸 ③硝酸铵固体 ④NaCl固体,其中能使a端液面人低于b端液面的是①②
①②
.(填序号)分析:右侧U型管中a端液面人低于b端液面,说明与U型管相连通的广口瓶内气体体积受到小试管加入物质的影响而发生气体体积膨胀,压强增大.
解答:解:①因烧碱溶于水时放热,溶液温度升高,瓶中气体温度升高,气体受热膨胀,使U型管右侧水面上升,使右侧U型管中a端液面人低于b端液面,故①正确;
②浓硫酸溶于水时放热,溶液温度升高,瓶中气体温度升高,气体受热膨胀,使U型管右侧水面上升,使右侧U型管中a端液面人低于b端液面,故②正确;
③硝酸钾溶于水吸热,溶液温度降低,瓶中气体温度降低,气体体积变小,使右侧U型管中a端液面人高于b端液面,故③错误;
④蔗糖溶于水时,热现象不明显,也就不能使U型管中的液面有明显变化,故④错误;
故答案为:①②
②浓硫酸溶于水时放热,溶液温度升高,瓶中气体温度升高,气体受热膨胀,使U型管右侧水面上升,使右侧U型管中a端液面人低于b端液面,故②正确;
③硝酸钾溶于水吸热,溶液温度降低,瓶中气体温度降低,气体体积变小,使右侧U型管中a端液面人高于b端液面,故③错误;
④蔗糖溶于水时,热现象不明显,也就不能使U型管中的液面有明显变化,故④错误;
故答案为:①②
点评:本题结合实验现象考查了化学反应中的热量变化,培养了学生分析问题、解决问题的能力.

练习册系列答案
 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 (2013?淄博二模)(1)写出Co2+离子基态的价电子排布式:
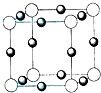
(2013?淄博二模)(1)写出Co2+离子基态的价电子排布式: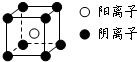 短周期元素A、B、C、D、E、F,原子序数依次增大.已知:①A与E同主族,E的单质与D2反应可生成E2D和E2D2两种固体;②F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;③CA4++DA-=CA3↑+A2D,各种反应和生成物的电子数都与E+相等.请回答下列问题:
短周期元素A、B、C、D、E、F,原子序数依次增大.已知:①A与E同主族,E的单质与D2反应可生成E2D和E2D2两种固体;②F的单质在D2中燃烧的产物可使品红溶液褪色;B的单质在D2中燃烧可生成BD和BD2两种气体;③CA4++DA-=CA3↑+A2D,各种反应和生成物的电子数都与E+相等.请回答下列问题:

 (2011?平顶山二模)A、B、C、D、E五种前四周期元素,原子序数依次增大.已知D元素原子核外的M层上有3个单电子存在.在周期表中,B、E与D同主族,A、C分别与B、D处于相邻位置.回答下列问题:
(2011?平顶山二模)A、B、C、D、E五种前四周期元素,原子序数依次增大.已知D元素原子核外的M层上有3个单电子存在.在周期表中,B、E与D同主族,A、C分别与B、D处于相邻位置.回答下列问题: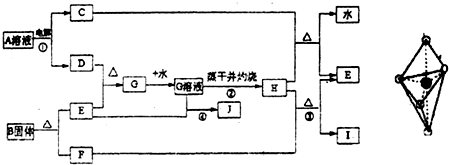
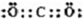
 I:氮元素可以形成多种化合物.回答以下问题:
I:氮元素可以形成多种化合物.回答以下问题: