题目内容
乙醇在与浓硫酸混合共热的反应过程中,受反应条件的影响,可发生两类不同的反应类型,如图1所示:
1,4二氧六环是一种常见的溶剂.它可以通过下列合成路线制得,如图2所示:
请回答:
(1)写出下列物质的结构简式.
A: ,B: ,C: .
(2)写出下列反应方程式,并注明反应类型.
A→B ,反应类型: ;
B→C ,反应类型: ;
如图3所示 ,反应类型: .
1,4二氧六环是一种常见的溶剂.它可以通过下列合成路线制得,如图2所示:
请回答:
(1)写出下列物质的结构简式.
A:
(2)写出下列反应方程式,并注明反应类型.
A→B
B→C
如图3所示

考点:有机物的推断
专题:
分析:采用逆推法分析:根据合成路线 结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,据此分析.
结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,据此分析.
 结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,据此分析.
结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,据此分析.解答:
解:(1)采用逆推法分析:根据合成路线 结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,故答案为:CH2=CH2;BrCH2CH2Br;HOCH2CH2OH;
结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,故答案为:CH2=CH2;BrCH2CH2Br;HOCH2CH2OH;
(2)反应A→B是乙烯与溴的加成反应,生成1,2-二溴乙烷,反应方程式为:CH2=CH2+Br2→BrCH2CH2Br,
反应B→C是卤代烃的水解,1,2-二溴乙烷在氢氧化钠溶液中水解生成乙二醇,反应方程式为:BrCH2CH2Br+2NaOH
HOCH2CH2OH+2NaBr,
乙二醇发生取代反应生成1,4二氧六环,反应方程式为:2HOCH2CH2OH
 +2H2O,
+2H2O,
故答案为:CH2=CH2+Br2→BrCH2CH2Br;加成反应;
BrCH2CH2Br+2NaOH
HOCH2CH2OH+2NaBr;取代反应(或水解反应);
2HOCH2CH2OH
 +2H2O;取代反应.
+2H2O;取代反应.
 结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,故答案为:CH2=CH2;BrCH2CH2Br;HOCH2CH2OH;
结合反应条件可知,C应该是乙二醇,C的结构简式为:HOCH2CH2OH,B是1,2-二溴乙烷,B的结构简式为:BrCH2CH2Br,故A是乙烯,CH2=CH2,故答案为:CH2=CH2;BrCH2CH2Br;HOCH2CH2OH;(2)反应A→B是乙烯与溴的加成反应,生成1,2-二溴乙烷,反应方程式为:CH2=CH2+Br2→BrCH2CH2Br,
反应B→C是卤代烃的水解,1,2-二溴乙烷在氢氧化钠溶液中水解生成乙二醇,反应方程式为:BrCH2CH2Br+2NaOH
| 水 |
乙二醇发生取代反应生成1,4二氧六环,反应方程式为:2HOCH2CH2OH
| 浓硫酸 |
 +2H2O,
+2H2O,故答案为:CH2=CH2+Br2→BrCH2CH2Br;加成反应;
BrCH2CH2Br+2NaOH
| 水 |
2HOCH2CH2OH
| 浓硫酸 |
 +2H2O;取代反应.
+2H2O;取代反应.
点评:有机物的合成是通过化学反应使有机物的碳链增长或缩短,或碳链和碳环的相互转变,或在碳链或碳环上引入或转换各种官能团,以制取不同类型、不同性质的有机物;有机合成题能较全面地考查学生的有机化学基础知识和逻辑思维能力、创造思维能力等.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
等质量的氯气与下列足量物质反应,转移的电子数最少的是( )
| A、冷的NaOH溶液 |
| B、SO2的水溶液 |
| C、FeCl2溶液 |
| D、铜 |
向某密闭容器中充入1mol CO和2mol H2O(g),发生反应:CO+H2O(g)
CO2+H2.当反应达到平衡时,CO的体积分数为x.若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是( )
| ||
| 高温 |
| A、0.5molCO+2molH2O(g)+1molCO2+1molH2 |
| B、1molCO+1molH2O(g)+1molCO2+1molH2 |
| C、0.5molCO+1.5molH2O(g)+0.4molCO2+0.4 molH2 |
| D、0.5molCO+1.5molH2O(g)+0.5molCO2+0.5molH2 |
如图为短周期的一部分,推断关于Y、Z、M说法正确的是( )


| A、非金属性:Y>Z>M |
| B、M2是由非极性共价键构成的分子 |
| C、原子半径:M>Z>Y |
| D、M单质常温下为无色气体 |
下列各元素的氧化物中,既能与盐酸反应,又能够与NaOH溶液反应的是( )
| A、元素X:它的原子中M层比L层少2个电子 |
| B、元素Y:它的二价阳离子核外电子总数与氩原子相同 |
| C、元素Z:位于元素周期表中的第三周期ⅢA 族 |
| D、元素W:它的焰色反应颜色呈黄色 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示,下列说法不正确的是( )


| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是蔗糖溶液 |
| C、利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol |
| D、途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 |
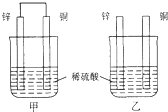 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.