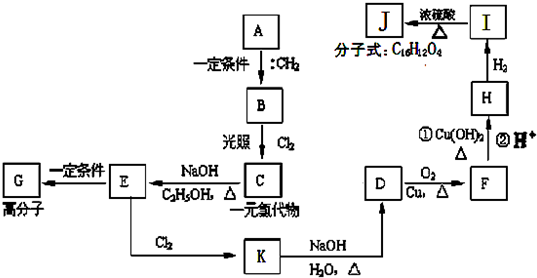
题目内容
下列说法错误的是( )
| A、钠是电和热的良导体 |
| B、在水中的溶解性:NaHCO3大于Na2CO3 |
| C、明矾净水是由于明矾在水中形成Al(OH)3胶体具有吸附作用 |
| D、某溶液焰色反应时,火焰呈黄色就说明该溶液一定有钠元素,一定没有钾元素 |
考点:钠的物理性质,盐类水解的原理,钠的重要化合物,焰色反应
专题:
分析:A、钠是金属具有金属通性;
B、碳酸钠溶解性大于碳酸氢钠;
C、明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用;
D、钾元素焰色反应需要隔着钴玻璃呈紫色,不隔着钴玻璃呈黄色不能判断钾元素的存在;
B、碳酸钠溶解性大于碳酸氢钠;
C、明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用;
D、钾元素焰色反应需要隔着钴玻璃呈紫色,不隔着钴玻璃呈黄色不能判断钾元素的存在;
解答:
解:A、钠是金属具有金属通性,导电导热延展性,钠是电和热的良导体,故A正确;
B、碳酸钠溶解性大于碳酸氢钠,故B错误;
C、明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水,故C正确;
D、钾元素焰色反应需要隔着钴玻璃呈紫色,不隔着钴玻璃呈黄色不能判断钾元素的存在,故D错误;
故选BD.
B、碳酸钠溶解性大于碳酸氢钠,故B错误;
C、明矾净水是利用铝离子水解生成氢氧化铝胶体具有吸附悬浮杂质的作用,可以净水,故C正确;
D、钾元素焰色反应需要隔着钴玻璃呈紫色,不隔着钴玻璃呈黄色不能判断钾元素的存在,故D错误;
故选BD.
点评:本题考查了钠及其化合物性质的分析应用,盐类水解分析判断,焰色反应的实质理解,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
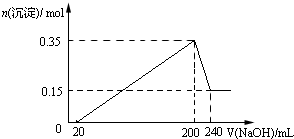 将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )
将一定质量的Mg和Al混合物投入到200mL稀硫酸中,固体全部溶解后,向所得溶液中滴加NaOH溶液至过量,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法不正确的是( )| A、Mg和Al的总质量为9g |
| B、最初20mLNaOH溶液用于中和过量的稀硫酸 |
| C、NaOH溶液物质的量浓度为5mol?L-1 |
| D、生成的氢气在标准状况下的体积为11.2L |
下列说法不正确的是( )
| A、麦芽糖及其水解产物均能发生银镜反应 |
| B、用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 |
| C、在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
D、用甘氨酸(H2N-CH2-COOH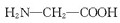 )和丙氨酸( )和丙氨酸(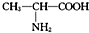 )缩合最多可形成4种二肽 )缩合最多可形成4种二肽 |
把CO2通入下列饱和溶液中,最终一定会有沉淀的是( )
| A、CaCl2 |
| B、Na2CO3 |
| C、Ca(OH)2 |
| D、NaNO3 |
设NA为阿佛加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA |
| B、同温同压下,体积相同的氢气和氩气所含的分子数不相等 |
| C、1L 2mol/L的氯化镁溶液中含氯离子为2NA |
| D、标准状况下22.4LH2O中分子数为NA |
下列微粒中,与OH-具有相同的质子数和相同的电子数的是( )
| A、F- |
| B、H2O |
| C、NH4+ |
| D、NH3 |
物质的量均为0.4mol的 Na、Mg、Al 分别与150ml 浓度为2mol/L的盐酸反应,相同温度和压强下比较产生H2的体积 ( )
| A、Na产生的多 |
| B、Mg产生的多 |
| C、Al产生的多 |
| D、一样多 |
下列说法中,正确的是( )
| A、△H>0表示放热反应,△H<0 表示吸热反应 |
| B、若反应△H>0;△S<0,则反应一定能自发进行 |
| C、1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
| D、热化学方程式中的化学计量数表示物质的量,所以可以是分数 |