题目内容
下图是用0.1000 mol·L-1 NaOH溶液滴定20.00 mL未知浓度盐酸(酚酞做指示剂)的滴定曲线。下列说法正确的是:
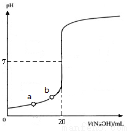
A.水电离出的氢离子浓度:a>b
B.盐酸的物质的量浓度为0.0100 mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00 mL时,该混合液的pH=1+lg3
D
【解析】
试题分析:a、b两点,酸均有剩余,氢离子浓度越大对水的电离抑制越强,所以水电离出的氢离子浓度:a<b,故A错误;等体积的盐酸和氢氧化钠溶液混合呈中性,则盐酸和氢氧化钠的浓度相同,故B错误;指示剂变色,且半分钟内颜色不再变化,达到滴定终点,故C错误;当滴加NaOH溶液10.00 mL时,所以盐酸的物质的量浓度为 mol/L,混合液的pH=1+lg3,故D正确。
mol/L,混合液的pH=1+lg3,故D正确。
考点:本题考查酸碱中和滴定。

 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案(10分)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要作用。
(1)真空碳热还原氯化法可实现由铝矿制备金属铝,其相关的热化学方程式如下:
①2Al2O3(s)+ 2AlCl3(g)+ 6C(s)=6AlCl(g)+ 6CO(g) △H=a kJ?mol-1
②3AlCl(g)= 2Al(l)+ AlCl3(g) △H=b kJ?mol-1
反应Al2O3(s)+ 3C(s)=2Al(l)+ 3CO(g)的△H= kJ?mol-1(用含a、b的代数式表示)。
(2)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+ 2NO(g) N2(g)+ CO2(g) △H=Q kJ?mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+ CO2(g) △H=Q kJ?mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
浓度 (mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.68 | 0.50 | 0.50 | 0.60 | 0.60 |
N2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
CO2 | 0 | 0.16 | 0.25 | 0.25 | 0.30 | 0.30 |
①T1℃时,该反应的平衡常数K=
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号)
a.通入一定量的NO b.加入一定量的活性炭
c.加入合适的催化剂 d.适当缩小容器的体积
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为3:1:1,则Q 0(填“>”或“<”)。
④在恒容绝热条件下,能判断该反应一定达到化学平衡状态的依据是
a.单位时间内生成2nmolNO(g)的同时消耗nmolCO2(g)
b.反应体系的温度不再发生改变
c.混合气体的密度不再发生改变
 时间(min)
时间(min) O2(g)===Na2O(s) ΔH1=-414 kJ·mol-1
O2(g)===Na2O(s) ΔH1=-414 kJ·mol-1