题目内容
有等质量的三种物质:①纯净的Na2CO3 a g;②Na2CO3与NaHCO3的混合物a g;③纯净的NaHCO3 a g,按要求回答下列问题:
(1)分别与盐酸完全反应时,耗酸量从大到小的顺序为: ;
(2)分别和盐酸完全反应时,放出CO2气体的量从大到小的顺序为: ;
(3)分别溶于水,再加入足量的澄清石灰水,生成沉淀的质量从大到小的顺序为: ;
(4)分别配成等体积的溶液,C(Na+)的浓度从大到小的顺序为: ;
(5)将ag Na2CO3和NaHCO3的混合物充分加热,其质量变为b g,则Na2CO3的质量分别为: ;
(6)若将题干中的等质量改为等物质的量,回答上述(1)(2)(3)(4)四问.
(1)分别与盐酸完全反应时,耗酸量从大到小的顺序为:
(2)分别和盐酸完全反应时,放出CO2气体的量从大到小的顺序为:
(3)分别溶于水,再加入足量的澄清石灰水,生成沉淀的质量从大到小的顺序为:
(4)分别配成等体积的溶液,C(Na+)的浓度从大到小的顺序为:
(5)将ag Na2CO3和NaHCO3的混合物充分加热,其质量变为b g,则Na2CO3的质量分别为:
(6)若将题干中的等质量改为等物质的量,回答上述(1)(2)(3)(4)四问.
考点:化学方程式的有关计算
专题:计算题
分析:等质量的三种物质:①纯净的Na2CO3 a g;②Na2CO3与NaHCO3的混合物a g;③纯净的NaHCO3 a g,分别算出它们物质的量,
(1)与盐酸完全反应时,分别列出Na2CO3、NaHCO3与盐酸反应的比例关系时,求出HCl的量.
(2)与盐酸完全反应时,分别列出Na2CO3、NaHCO3与生成CO2的比例关系时,求出CO2的量
(3)加入足量的澄清石灰水,分别列出Na2CO3、NaHCO3与生成CaCO3的比例关系时,求出CaCO3的量
(4)Na2CO3、NaHCO3的中的n(Na+)的大小
(5)将ag Na2CO3和NaHCO3的混合物充分加热,NaHCO3的分解方程式,据差量法解题
(6)若将题干中的等质量改为等物质的量,类似上面的方法可求解.
(1)与盐酸完全反应时,分别列出Na2CO3、NaHCO3与盐酸反应的比例关系时,求出HCl的量.
(2)与盐酸完全反应时,分别列出Na2CO3、NaHCO3与生成CO2的比例关系时,求出CO2的量
(3)加入足量的澄清石灰水,分别列出Na2CO3、NaHCO3与生成CaCO3的比例关系时,求出CaCO3的量
(4)Na2CO3、NaHCO3的中的n(Na+)的大小
(5)将ag Na2CO3和NaHCO3的混合物充分加热,NaHCO3的分解方程式,据差量法解题
(6)若将题干中的等质量改为等物质的量,类似上面的方法可求解.
解答:
解:等质量的三种物质:①纯净的Na2CO3 a g,物质的量为
mol;②Na2CO3与NaHCO3的混合物a g,物质的量为
mol~
mol之间;③纯净的NaHCO3 a g,物质的量为
mol
(1)与盐酸完全反应时,据Na2CO3------------2HCl、NaHCO3------------HCl
mol
mol
mol
mol
故答案为:①>②>③;
(2)与盐酸完全反应时,据Na2CO3------------CO2、NaHCO3------------CO2
mol
mol
mol
mol
故答案为:③>②>①;
(3)加入足量的澄清石灰水,据Na2CO3------------CaCO3↓、NaHCO3------------CaCO3↓
mol
mol
mol
mol
故答案为:③>②>①;
(4)Na2CO3中的n(Na+)=2×
mol=
mol,的大小、NaHCO3中的n(Na+)=
mol,又因为配成的是等体积的溶液,
故答案为:①>②>③;
(5)将ag Na2CO3和NaHCO3的混合物充分加热,据2NaHCO3
Na2CO3+CO2↑+H2O△m
168 62
(a-b)g (a-b)g
则Na2CO3的质量分别为:ag-
(a-b)g=(
b-
a)g,故答案为:(
b-
a)g;
(6)若将题干中的等质量改为等物质的量,设为1mol
(1)与盐酸完全反应时,据Na2CO3------------2HCl、NaHCO3------------HCl
1mol 2mol 1mol 1mol
故答案为::①>②>③;
(2)与盐酸完全反应时,据Na2CO3------------CO2、NaHCO3------------CO2
1mol 1mol 1mol 1mol
故答案为:①=②=③;
(3)加入足量的澄清石灰水,据Na2CO3------------CaCO3↓、NaHCO3------------CaCO3↓
1mol 1mol 1mol 1mol
故答案为:①=②=③;
(4)Na2CO3中的n(Na+)=2×1mol=2mol,的大小、NaHCO3中的n(Na+)=1mol,又因为配成的是等体积的溶液,
故答案为:①>②>③.
| a |
| 106 |
| a |
| 106 |
| a |
| 84 |
| a |
| 84 |
(1)与盐酸完全反应时,据Na2CO3------------2HCl、NaHCO3------------HCl
| a |
| 106 |
| a |
| 53 |
| a |
| 84 |
| a |
| 84 |
故答案为:①>②>③;
(2)与盐酸完全反应时,据Na2CO3------------CO2、NaHCO3------------CO2
| a |
| 106 |
| a |
| 106 |
| a |
| 84 |
| a |
| 84 |
故答案为:③>②>①;
(3)加入足量的澄清石灰水,据Na2CO3------------CaCO3↓、NaHCO3------------CaCO3↓
| a |
| 106 |
| a |
| 106 |
| a |
| 84 |
| a |
| 84 |
故答案为:③>②>①;
(4)Na2CO3中的n(Na+)=2×
| a |
| 106 |
| a |
| 53 |
| a |
| 84 |
故答案为:①>②>③;
(5)将ag Na2CO3和NaHCO3的混合物充分加热,据2NaHCO3
| ||
168 62
| 84 |
| 31 |
则Na2CO3的质量分别为:ag-
| 84 |
| 31 |
| 84 |
| 31 |
| 53 |
| 31 |
| 84 |
| 31 |
| 53 |
| 31 |
(6)若将题干中的等质量改为等物质的量,设为1mol
(1)与盐酸完全反应时,据Na2CO3------------2HCl、NaHCO3------------HCl
1mol 2mol 1mol 1mol
故答案为::①>②>③;
(2)与盐酸完全反应时,据Na2CO3------------CO2、NaHCO3------------CO2
1mol 1mol 1mol 1mol
故答案为:①=②=③;
(3)加入足量的澄清石灰水,据Na2CO3------------CaCO3↓、NaHCO3------------CaCO3↓
1mol 1mol 1mol 1mol
故答案为:①=②=③;
(4)Na2CO3中的n(Na+)=2×1mol=2mol,的大小、NaHCO3中的n(Na+)=1mol,又因为配成的是等体积的溶液,
故答案为:①>②>③.
点评:本题考查Na2CO3和NaHCO3性质的异同,主要考查反应的定量关系计算和比较.

练习册系列答案
相关题目
按如图装置进行实验(N装置中两个电极均为石墨棒),下列描述正确的是( )

| A、a、b未连接时,装置N中C1电极上有气体析出 |
| B、不论a、b是否连接,装置M中观察到的实验现象相同 |
| C、a、b连接,工作一段时间后装置M中溶液pH变大,装置N中溶液pH变小 |
| D、a、b连接,装置M中若有0.1molSO42-移到Cu电极,装置N中C2极放出H22.24L(标准状况) |
下列过程因发生取代反应而产生的是( )
| A、乙烯使溴的四氯化碳溶液褪色 |
| B、将苯加入溴水中,振荡后水层接近无色 |
| C、将苯、浓硫酸、浓硝酸混合后在50℃-60℃水浴中加热 |
| D、液态植物油与氢气反应生成固态物质 |
下列溶液中的氯离子浓度与50mL 1mol/L的AlCl3溶液中氯离子浓度相等的是( )
| A、50 mL 1 mol/L的NaCl |
| B、100 mL 3 mol/L的NH4Cl |
| C、75 mL 2 mol/L的KCl |
| D、75 mL 2 mol/L的CaCl2 |
下列说法正确的是( )
| A、利用太阳能将海水蒸馏得到淡水,使太阳能转化成了化学能 |
| B、煤的气化就是将煤转化为可燃性气态的过程,是化学变化 |
| C、淀粉、蛋白质和油脂都是高聚物,在一定条件下都能水解 |
| D、石油裂解可以得到更多的汽油,这种汽油是一种纯净物 |
下列物质中只有离子键的是( )
| A、O2 |
| B、NaOH |
| C、H2O |
| D、NaCl |
下列化学用语正确的是( )
A、硫原子的原子结构示意图: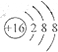 | ||
B、CH4分子的比例模型: | ||
| C、乙烯的结构简式:CH2CH2 | ||
D、原子核内有10个中子的氧原子:
|
 和
和 ;③氧气(O2)与臭氧(O3);④D与T;
;③氧气(O2)与臭氧(O3);④D与T;
