题目内容
18.已知Co2O3在酸性溶液中易被还原成Co2+;且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )| A. | Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3 | |
| B. | 每1mol Co2O3在酸性溶液中被还原生成Co2+时转移2 mol e- | |
| C. | FeCl3溶液能使淀粉-KI试纸变蓝 | |
| D. | I2具有较弱的氧化性,不可以将Co2+氧化成Co2O3 |
分析 根据化学方程式,只要根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性得出的结果符合题干已知条件的,说明反应成立.
解答 解:A、因为氧化性FeCl3>I2,所以不能生成FeI3,则反应不能发生,故A选;
B、Co元素的化合价从+3降低到+2,转移一个电子,所以每1mol Co2O3在酸性溶液中被还原生成Co2+时转移2 mol e-,故B不选;
C、因为氧化性FeCl3>I2,所以FeCl3溶液能把KI氧化为I2,则FeCl3溶液能使淀粉-KI试纸变蓝,故C不选;
D、已知氧化性:Co2O3>I2,所以I2不可以将Co2+氧化成Co2O3,故D不选;
故选A.
点评 本题考查学生分析和解决问题的能力,可以根据氧化剂的氧化性大于氧化产物的氧化性,难度不大,明确反应中元素的化合价变化是解答本题的关键.

练习册系列答案
相关题目
8.甲同学用米汤(内含淀粉)给乙同学写信,乙同学收到信后,为了看清信中的内容,应使用的化学试剂是( )
| A. | 碘化钾 | B. | 淀粉碘化钾溶液 | C. | 碘酒 | D. | 溴水 |
9.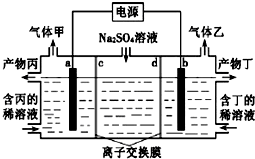 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极.测得同温同压下,气体甲与气体乙的体积比约为1:2,以下说法不正确的是( )| A. | a极与电源的正极相连 | |
| B. | 产物丙为硫酸溶液 | |
| C. | 离子交换膜d为阳离子交换膜(允许阳离子通过) | |
| D. | a电极反应式为2H2O+2e-═2OH-+H2↑ |
6.某溶液中加入KSCN溶液无明显现象,再通入氯气,溶液立即变为红色,说明原溶液中一定含有( )
| A. | Fe3+ | B. | Fe2+ | C. | Cu2+ | D. | Zn2+ |
10.在一定的温度下,下列叙述与图象对应正确的是( )
| A. |  曲线可表示向0.1 mol/L CH3COONa溶液中加水稀释的过程中OH-浓度随溶液体积的变化趋势 | |
| B. | 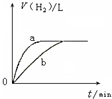 曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)跟同浓度等体积盐酸反应过程中产生H2体积的变化趋势 | |
| C. |  曲线c、d分别表示等质量的铝分别跟过量烧碱溶液、过量盐酸反应过程中产生H2体积的变化趋势 | |
| D. | 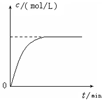 曲线可表示足量锌与一定量稀醋酸反应过程中,Zn2+浓度的变化趋势(假设反应过程中溶液体积保持不变) |
7.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 无色溶液中:Cr2O${\;}_{7}^{2-}$、Fe3+、SCN-、Cl- | |
| B. | 能使石蕊呈蓝色的溶液中:Na+、K+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ | |
| C. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012 的溶液中:S2O${\;}_{3}^{2-}$、CrO${\;}_{4}^{2-}$、Cl-、Mg2+ | |
| D. | 水电离的c (H)=10-12mol•L-1 的溶液中:HCO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$、Cu2+、NH${\;}_{4}^{+}$ |
8.下列说法不正确的是( )
| A. | 由于电流的作用,酸、碱、盐溶于水发生电离 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸,不能透过半透膜 | |
| C. | 存在自由移动的离子是电解质溶液导电的原因 | |
| D. | 向氢氧化铁胶体中滴加稀硫酸,开始时产生沉淀,继续滴加时沉淀溶解 |