题目内容
15.为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、盐酸和K2CO3三种试剂,按如图步骤操作: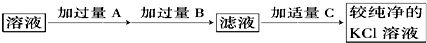
(1)写出三种试剂的化学式:ABa(OH)2,BK2CO3,CHCl.
(2)加过量A的原因是:为了除尽Mg2+和SO42-,有关反应的化学方程式为:MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓
(3)加过量B的原因是:为了除尽过量的Ba2+.
分析 除去KCl溶液中的少量MgCl2和MgSO4,可看成把Mg2+、SO42-沉淀而除去,因此A选择所提供试剂中的Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2可加入B即所选试剂中的K2CO3而除去;最后通过滴加C盐酸可把过量的K2CO3及反应生成的KOH同时反应掉而生成KCl,以此来解答.
解答 解:除去KCl溶液中的少量MgCl2和MgSO4,可看成把Mg2+、SO42-沉淀而除去,因此A选择所提供试剂中的Ba(OH)2可同时沉淀掉Mg2+、SO42-离子;反应生成的BaCl2和过量的Ba(OH)2可加入B即所选试剂中的K2CO3而除去;最后通过滴加C盐酸可把过量的K2CO3及反应生成的KOH同时反应掉而生成KCl,
(1)由上述分析可知,A、B、C分别为Ba(OH)2、K2CO3、HCl,故答案为:Ba(OH)2;K2CO3;HCl;
(2)为确保混合溶液中的MgCl2和MgSO4全部反应而沉淀掉,故应加入过量的Ba(OH)2,生成Mg(OH)2、BaSO4,发生的反应为MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓,
故答案为:为了除尽Mg2+和SO42-;MgCl2+Ba(OH)2=Mg(OH)2↓+BaCl2、MgSO4+Ba(OH)2=BaSO4↓+Mg(OH)2↓;
(3)为确保溶液是的Ba2+全部沉淀而除去,应加入过量的K2CO3到沉淀不再产生,反应生成碳酸钡沉淀、氢氧化钾,故答案为:为了除尽过量的Ba2+.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应、混合物分离提纯为解答的关键,侧重分析与应用能力的考查,注意元素化合物的性质,题目难度不大.

| A. | 用铁与稀硝酸反应来制备氢气 | |
| B. | SO2能使湿润的蓝色石蕊试纸先变红后褪色 | |
| C. | NO2溶于水发生了氧化还原反应,它既是氧化剂又是还原剂 | |
| D. | 等质量的碳酸钠、碳酸氢钠分别与足量的盐酸反应,前者产生的二氧化碳多 |
| A. | Na | B. | P | C. | Cl | D. | F |
| A. | 将Ba(OH)2溶液不断加入KAl(SO4)2溶液中反应至沉淀物质的量最大:3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ | |
| B. | Cl2通入冷水中:Cl2+H2O═Cl-+ClO-+2H+ | |
| C. | CuSO4溶液跟Ba(OH)2溶液混合:Ba2++SO42-═BaSO4↓ | |
| D. | 漂白粉溶液中通入足量SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO |
| A. | NaHSO3 | B. | Cu2(OH)2CO3 | C. | Ca(HCO3)2 | D. | NH4NO3 |


 [来
[来 化学方程式:② 。
化学方程式:② 。