��Ŀ����
��ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���
CO(g) +2H2(g)  CH3OH(g)
��H
CH3OH(g)
��H
��1���жϷ�Ӧ�ﵽƽ��״̬�������� ������ţ���
a�� ����CH3OH������������CO���������
b�� ���������ܶȲ���
c�� �������������ʵ�������
d�� CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
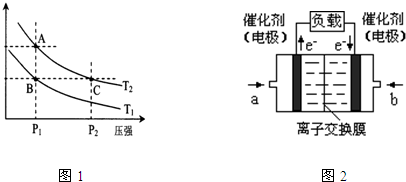
��2��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ1��

�ٸ÷�Ӧ��H___0���������������
��ʵ����������������250�桢1.3��104 kPa���ң�ѡ���ѹǿ��������_______��
��3����ͼ2��ʾ���¶ȷֱ�ΪT1��T2ʱ��ƽ����ϵ��H2�����������ѹǿ�仯���ߣ�A��C����ķ�Ӧ����A____C�����������������������ͬ����A��C����Ļ�ѧƽ�ⳣ��A_____C����״̬B��״̬A���ɲ���______�ķ���������¡����¡�����

��4��һ�������£�0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�Q KJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
��5��ͼ3�Ǽ״�ȼ�ϵ�أ��������ҺΪKOH��Һ���ṹʾ��ͼ��д�� a���缫�Ϸ����ĵ缫��Ӧʽ ��

��1��c d ��2�֣�
��2���� ����2�֣� ����1.3��104Kpa�£�COת�����ѽϸߣ�������ѹǿCOת������߲��������ɱ����ӣ��ʵò���ʧ����2�֣�
��3������=�����£���6�֣���2�֣�
��4��2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(l) ��H=-4Q kJ/mol��3�֣�
��5��CH3OH-6e-+8OH- =CO32-+6H2O��3�֣�
��������
�����������1��a������CH3OH������������CO�����ʶ�������Ӧ���ʣ��������ж�ƽ������ݣ�b����Ϊ���������غ㣬�������ݣ��ܶ�Ϊ��ֵ�����ܶȲ��䲻����Ϊ�ж�ƽ������ݣ�c����Ӧǰ�������ϵ�����ȣ����Ի������������ʵ�������˵����Ӧ�ﵽƽ�⣻d����Ӧ���������Ũ�Ȳ��䣬��˵����Ӧ�ﵽƽ�⡣
��2���١��¶����ߣ�CO��ת���ʼ�С��˵������ӦΪ���ȷ�Ӧ����∆H<0��
�ڡ�����ͼʾ��֪��1.3��104Kpa�£�COת�����ѽϸߣ�������ѹǿCOת������߲�������ѹǿ����Ҫ��ǿ�����豸�ͷ�Ӧװ�õĿ�ѹ�����������ɱ����ӣ��ò���ʧ��
��3��A��C���¶���ͬ��C��ѹǿ����Ӧ���ʿ죻�¶Ȳ��䣬ƽ�ⳣ����ȣ�A��H2�����������Ϊ����ӦΪ���ȷ�Ӧ������A���¶ȸ���B�㣬��״̬B��Ϊ״̬A�����¡�
��4��д���״�ȼ�յĻ�ѧ����ʽ��ע��״̬����ΪCH3CH2OH��ϵ��Ϊ2�����H=-4Q kJ•mol‾1���ɵ��Ȼ�ѧ����ʽ��
��5����Ϊ�������ҺΪKOH��Һ��CH3OH��OH‾���ڵ�������ʧȥ��������CO32‾��H2O����ƽ�ɵõ缫����ʽ��CH3OH-6e-+8OH- =CO32-+6H2O��
���㣺���⿼���жϷ�Ӧ�Ƿ�ƽ������ݡ���ѧ��Ӧ����ЧӦ��������ƽ���Ӱ�졢�Ȼ�ѧ����ʽ����д ���缫����ʽ����д��

 CH3OH��g����H
CH3OH��g����H