题目内容
15.H2O2在工业、农业、医药上都有广泛的用途.(1)H2O2是二元弱酸,写出第一步的电离方程式H2O2?H++HO2-,第二步的电离平衡常数表达式Ka2=$\frac{c({H}^{+})c({{O}_{2}}^{2-})}{c(H{{O}_{2}}^{-})}$.
(2)许多物质都可以做H2O2分解的催化剂.一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化).下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是①④.
①I- ②Fe3+ ③Cu2+ ④Fe2+
(3)用碱性氢氧燃料电池合成H2O2,具有效率高,无污染等特点.电池总反应为:H2+O2+OH-=H2O+HO2-.写出正极反应式:O2+H2O+2e-=HO2-+OH-.
(4)H2O2是一种环境友好的强氧化剂.电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+ 等)制备硫酸镍的一种流程如下:
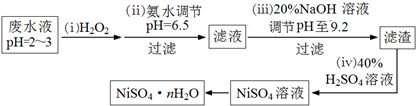
①第(ⅰ)步,加入H2O2反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
②第(ⅱ)步,滤渣中的主要成分在医疗上的用途是尿糖的检测.
分析 (1)H2O2为二元弱酸,分2步电离;平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积;
(2)根据在反应过程中先被氧化,后被还原的即化合价先升高,后降低,结合元素的化合价来解答;
(3)碱性氢氧燃料电池工作时,电解质溶液是KOH溶液(碱性电解质),正极是O2得到电子,发生还原反应,正极的电极反应式为:O2+H2O+2e-=HO2-+OH-;
(4)①根据双氧水有强氧化性,能氧化还原性的物质,如Fe2+;
②Cu2+能与氨水反应生成氢氧化铜沉淀,氢氧化铜可用于检验尿糖.
解答 解:(1)H2O2为二元弱酸,分2步电离,电离方程式分别为:H2O2?H++HO2-,HO2-?H++O22-,第二步的电离平衡常数表达式Ka2=$\frac{c({H}^{+})c({{O}_{2}}^{2-})}{c(H{{O}_{2}}^{-})}$,
故答案为:H2O2?H++HO2-;$\frac{c({H}^{+})c({{O}_{2}}^{2-})}{c(H{{O}_{2}}^{-})}$;
(2)①I-的化合价可先升高到0价,再降低到-1价,符合题意;
②Fe3+的化合价只能先降低,然后再升高,不符合题意;
③Cu2+的化合价只能先降低,然后再升高,不符合题意,
④Fe2+的化合价可先升高到+3价,再降低到+2价,符合题意,
故选①④,
故答案为:①④;
(3)碱性氢氧燃料电池工作时,正极是O2得到电子,发生还原反应,电极反应式为O2+H2O+2e-=HO2-+OH-,
故答案为:O2+H2O+2e-=HO2-+OH-;
(4)①双氧水有强氧化性,能氧化Fe2+,离子方程式为:2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②滤渣中的主要成分是氢氧化铜,氢氧化铜在医疗上的用途是检验尿糖,故答案为:尿糖的检测.
点评 本题是一道综合知识题目,涉及实验操作,电离方程式式、平衡常数、氧化还原反应,原电池,考查学生分析和解决问题的能力,题目难度中等.

 快乐5加2金卷系列答案
快乐5加2金卷系列答案| A. | 分别通入酸性KMnO4溶液中 | B. | 分别点燃观察火焰 | ||
| C. | 分别通入澄清石灰水中 | D. | 分别通入溴水中 |
| A. | 2s | B. | 5f | C. | 2d | D. | 3px |
| A. | 一定是一种单质 | B. | 一定是纯净物 | ||
| C. | 可能是混合物也可能是纯净物 | D. | 一定是同位素组成的不同单质 |
| A. | 工业上将NH3与CO2在高温高压下制成[CO(NH2)2] | |
| B. | 空气中的O2和N2在闪电时化合成NO | |
| C. | 豆科植物的根瘤菌把氮气变为NH3 | |
| D. | 工业上用N2和H2来合成NH3 |
| A. | H2O2的结构式:H-O-O-H | B. | C2H4的结构简式:CH2CH2 | ||
| C. | O2-结构示意图: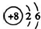 | D. | CCl4的结构式: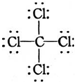 |
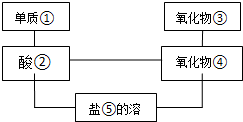 给图中①~⑤选择适当的物质,使有连线的两物质能发生反应.供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉.
给图中①~⑤选择适当的物质,使有连线的两物质能发生反应.供选择的试剂有稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉.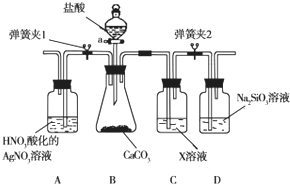 某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).
某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验).