题目内容
19.某科研小组采集到两种铜矿标本,经地理老师辨认为孔雀石和石青,老师说其化学组成均可表示为xCuCO3•yCu(OH)2,属于天然碳酸盐类铜矿.(1)为了准确测定两种矿石的化学组成,该小组同学将两种矿石分别与足量盐酸反应,孔雀石耗用的盐酸的物质的量与生成的CO2的物质的量之比为4:1;石青则为3:1.
请确定它们的化学组成,孔雀石:CuCO3•Cu(OH)2;石青:2CuCO3•Cu(OH)2.
(2)现取两份等质量的两种矿石的混合物样品,一份加入过量盐酸,生成CO2 6.6g;对另一份样品加热使其完全分解,得到CuO 20g,则混合物中孔雀石和石青的物质的量之比为1:1.
分析 (1)用孔雀石耗用的盐酸与生成的CO2的物质的量比为4:1,计算出化学组成可表示为xCuCO3•yCu(OH)2中x、y的比,再根据x、y为正整数且x≤2,y≤2的限制条件,推断出两物质的化学组成;发生反应:xCuCO3•yCu(OH)2+(2x+2y)HCl═(x+y)CuCl2+xCO2↑+(x+2y)H2O,计算出化学组成可表示为xCuCO3•yCu(OH)2中x、y关系,再根据x、y为正整数且x≤2,y≤2的限制条件解答;
(2)设孔雀石和石青的物质的量分别为amol、bmol,根据方程式表示出生成的二氧化碳、CuO,列方程计算解答.
解答 解:(1)根据孔雀石耗用的盐酸与生成的CO2的物质的量比为4:1,
和化学方程式xCuCO3•yCu(OH)2+2(x+y)HCl→(x+y)CuCl2+xCO2↑+(x+2y)H2O
可知:2(x+y):x=4:1,可得x:y=1:1,
∵x、y为正整数且x≤2,y≤2,
∴孔雀石的化学式可表示为CuCO3•Cu(OH)2;
而石青发生反应:xCuCO3•yCu(OH)2+(2x+2y)HCl═(x+y)CuCl2+xCO2↑+(x+2y)H2O,石青耗用的盐酸与生成的CO2的物质的量比为3:1,则(2x+2y):x=3:1,解得x=2y,
∵x、y为正整数且x≤2,y≤2,故x=2、y=1,
∴石青的化学式可表示为2CuCO3•Cu(OH)2,
故答案为:CuCO3•Cu(OH)2;2CuCO3•Cu(OH)2;
(2)设孔雀石和石青的物质的量分别为amol、bmol,则:
CuCO3•Cu(OH)2+4HCl═2CuCl2+CO2↑+3H2O
1 1
amol amol
2CuCO3•Cu(OH)2+6HCl═3CuCl2+2CO2↑+4H2O
1 2
bmol 2bmol
CuCO3•Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O
1mol 160g
amol 160ag
2CuCO3•Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+2CO2↑+H2O
1mol 240
bmol 240bg
则a+2b=$\frac{6.6g}{44g/mol}$,160ag+240bg=20g,
解之得a=0.05,b=0.05
该混合物中孔雀石和石青的物质的量之比=0.05mol:0.05mol=1:1,
答:孔雀石和石青的物质的量之比为1:1.
点评 本题考查化学式的推断、化学反应方程式的计算,注意根据方程式进行计算解答,题目难度中等,侧重于考查学生的分析能力和计算能力.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案| 选项 | 反应叙述 | 产物图示 |
| A | NaOH溶液与SO2 反应时溶液中的溶质 |  |
| B | NaAlO2溶液与盐酸反 应后铝元素的存在形式 |  |
| C | Fe和稀HNO3反应 后,铁元素的存在形式 | 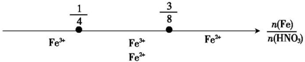 |
| D | Fe在Cl2中的燃烧产物 |  |
| A. | A | B. | B | C. | C | D. | D |
(1)合成氨的原料气N2和H2通常是以焦炭、水和空气为原料来制取的.其主要反应是:①2C+O2→2CO ②C+H2O(g)→CO+H2 ③CO+H2O(g)→CO2+H2
某次生产中将焦炭、H2O(g)和空气(设空气中N2和O2的体积比为4:1,下同)混合反应,所得气体产物经分析,组成如下表:则表中x=44m3.
| 气体 | CO | N2 | CO2 | H2 | O2 |
| 体积(m3)(标准状况) | x | 20 | 12 | 60 | 1.0 |
N2(g)+O2(g)?2NO(g)△H>0
若1mol空气含有0.8molN2和0.2molO2,1300℃时在密闭容器内反应达到平衡.测得NO为8×10-4mol.计算该温度下的平衡常数K=4×10-6;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是温度升高,反应速率加快,平衡右移.
(3)SO2和氮的氧化物都是空气中的有害气体,已知:
2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1
2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ•mol-1
则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=-41.8kJ•mol-1.
(4)25℃时,电离平衡常数:
| 化学式 | H2CO3 | HClO | H2C4H4O6(酒石酸) |
| 电离平衡常数 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=9.1×10-4 K2=4.3×10-5 |
a.常温下,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,所得溶液中各种离子浓度关系不正确的是AD
A.c(Na+)>c(ClO-)>c(HCO3-)>c(OH-)
B.c(Na+)>c(HCO3-)>c(ClO-)>c(H+)
C.c(Na+)═c(HClO)+c(ClO-)+c(HCO3-)+c(H2CO3)+c(CO32-)
D.c(Na+)+c(H+)═c(ClO-)+c(HCO3-)+2c(CO32-)
E.c(HClO)+c(H+)+c(H2CO3)═c(OH-)+c(CO32-)
b.常温下,0.1mol/L的酒石酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC4H4O6-)+2c(C4H4O62-)=(0.05+10-6-10-8)mol/L.(列出计算式)
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,该反应中Q>0 (选填“>”或“<”).
(2)能判断该反应已达到化学平衡状态的依据是cd.
a.容器中压强不变 b.反应热不变 c.v正(H2)=v逆(CO) d.CO2的质量分数不变
(3)800℃,在固定容积的密闭容器中加入混合物,起始浓度为c(CO)=0.01mol/L,c(H2O)=0.05mol/L,c(CO2)=0.01mol/L,c(H2)=0.03mol/L,反应开始时,H2O的消耗速率比生成速率大(填“大”或“小”).
(4)温度为850℃时,可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)在固定容积的密闭容器中进行,容器内物质的浓度变化如表:
850℃时物质的浓度(mol/L)的变化
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | O.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4min~5min之间,平衡向逆反应方向移动,可能的原因是d,表中5min~6min之间数值发生变化,可能的原因是a.
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度.
 一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )
一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入1molN2,右边充入CO和CO2的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )| A. | 右边CO与CO2分子数之比为1:3 | |
| B. | 右侧气体密度是相同条件下氢气密度的18倍 | |
| C. | 右侧CO的质量为1.75g | |
| D. | 若隔板处于距离右端$\frac{1}{6}$处,其他条件不变,则前后两次压强之比为25:24 |
| t/min n/mol | 0min | 2min | 4min | 6min | 8min |
| n(X) | 0.2 | 0.15 | 0.1 | 0.1 | 0.05 |
| n(Y) | 0.6 | 0.45 | 0.3 | 0.3 | 0.5 |
| n(Z) | 0 | 0.1 | 0.2 | 0.2 | 0.3 |
(2)在相同温度下,若1L容器为体积可变的密闭容器,现充入0.2mol X、0.6molY,达到平衡时n(Z)=bmol,则b>0.2(填“<”、“>”或“=”),平衡时容器的体积V=$\frac{4-5b}{4}$L(用含b的式子表示)
(3)维持温度和压强不变,第6min的平衡体系中再通入0.2molX和0.6molY,达到新平衡时Z的物质的量0.4mol
(4)维持温度和体积不变,在第6min的平衡体系中再通入0.2molX和0.6molY,达到新平衡时Z的体积分数增大(填“增大”、“减小”或“不变”)
| A. | 标准状况下,2.24 LCCl4中含Cl原子数目等于0.4NA | |
| B. | 2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA | |
| C. | 常温常压下,10 g 46%酒精水溶液中含氧原子总数为0.1NA | |
| D. | 1 mol甲基(-CH3)中含有电子的数目为10NA |