题目内容
14.下列金属冶炼原理错误的是( )| A. | 2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ | B. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2 | ||
| C. | MgO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+H2O | D. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ |
分析 金属冶炼的方法主要有:热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A、金属钠是活泼金属,工业上采用电解熔融物的方法冶炼,故A正确;
B、工业上采用热还原法来冶炼金属铁,故B正确;
C、金属镁是活泼金属,工业上采用电解熔融氯化镁的方法冶炼,故C错误;
D、对于不活泼金属Hg,可以直接用加热分解的方法将金属从氧化汞中还原出来,故D正确.
故选C.
点评 本题考查了金属冶炼的一般原理,难度不大,注意根据金属的活泼性不同采取相应的冶炼方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.下列物质中,既有离子键又有共价键的是( )
| A. | MgCl2 | B. | NH3 | C. | NH4Cl | D. | C2H2 |
5.下列关于有机物的说法正确的是( )
| A. | 天然气为纯净物 | |
| B. | 天然气是不可再生的能源 | |
| C. | 乙烯的结构简式为CH2CH2 | |
| D. | 过量的CH4和Cl2在光照条件下反应只生成CH3Cl |
9.下列物质在一定条件下能和氢氧化钠溶液发生反应的是( )
| A. | 汽油 | B. | 色拉油 | C. | 甘油 | D. | 机油 |
19. 某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
①锌为正极,铜为负极?
②电解质溶液的pH不变?
③电流表的指针发生偏转?
④铜极上有气泡产生?
⑤锌极上仍有少量气泡产生?
⑥溶液中的阳离子向负极移动.
 某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( )
某同学按如图所示的装置做实验,并记录实验情况.你认为框内叙述合理的是( ) ①锌为正极,铜为负极?
②电解质溶液的pH不变?
③电流表的指针发生偏转?
④铜极上有气泡产生?
⑤锌极上仍有少量气泡产生?
⑥溶液中的阳离子向负极移动.
| A. | ①②③ | B. | ③④⑤ | C. | ③④⑥ | D. | ②③④ |
6.下列物质能通过化合反应直接制得的是( )
①FeCl2 ②Fe(OH)3 ③NH4NO3 ④HCl.
①FeCl2 ②Fe(OH)3 ③NH4NO3 ④HCl.
| A. | 只有①②③ | B. | 只有②③ | C. | 只有①③④ | D. | 全部 |
3.X、Y两元素可形成XY3型共价化合物,则X、Y最外层的电子排布可能是( )
| A. | X:3s23p1 Y:3s23p4 | B. | X:2s22p3 Y:2s22p4 | ||
| C. | X:3s23p1 Y:2s22p5 | D. | X:2s22p3 Y:1s1 |
18. 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
 金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )
金属(M)-空气电池(如图)具有原料易得,能量密度高等优点,有望成为新能源汽车和移动设备的电源,该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH)n,己知:电池的“理论比能量”指单位质量的电极材料理论上能释放出的最大电能,下列说法不正确的是( )| A. | 采用多孔电极的目的是提高电极与电解质溶液的接触面积,并有利于氧气扩散至电极表面 | |
| B. | 在Mg-空气电池中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 | |
| C. | M-空气电池放电过程的正极反应式:正极反应式为O2+2H2O+4e-═4OH- | |
| D. | 比较Mg、Al、Zn三种金属-空气电池,Mg-空气电池的理论比能量最高 |
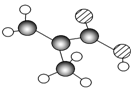 某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键). .
. .
.