题目内容
3.下列说法错误的是( )| A. | 钠元素性质活泼,不可能应用在电光源上 | |
| B. | 漂白粉的有效成分是Ca(ClO)2 | |
| C. | 浓硝酸可以盛放在铝制容器中 | |
| D. | 向3mL1mol/L的碳酸钠溶液中逐滴滴入稀盐酸,起初并无气体生成 |
分析 A.钠的焰色反应成黄色,黄色光的射程远,透雾能力强;
B.漂白粉是氯化钙和次氯酸钙的混合物,有效成分为次氯酸钙;
C.常温下铝在浓硝酸中发生钝化现象;
D.盐酸量少,碳酸钠溶液中滴入盐酸生成碳酸氢钠.
解答 解:A.高压钠灯发出的黄光射程远,透雾力强,对道路平面的照明度比高压水银灯高几倍,故将钠应用于电光源上,故A错误;
B.漂白粉是氯化钙和次氯酸钙的混合物,有效成分为次氯酸钙和二氧化碳、水蒸气反应生成次氯酸具有漂白作用和强氧化性,故B正确;
C.常温下铝在浓硝酸中发生钝化现象,生成致密氧化物薄膜阻止反应进行,浓硝酸可以盛放在铝制容器中,故C正确;
D.向3mL1mol/L的碳酸钠溶液中逐滴滴入稀盐酸,生成碳酸氢钠,起初无二氧化碳气体生成,故D正确;
故选A.
点评 本题考查了物质性质和应用,注意知识的积累,掌握基础是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.下列各组物质中,化学键类型完全相同的是( )
| A. | HI和NaI | B. | CS2和CO2 | C. | Cl2和CCl4 | D. | F2和NaBr |
11.用下列实验装置进行相应实验,能达到实验目的是( )
| A. | 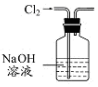 用图所示装置除去Cl2中含有的少量HCl | |
| B. | 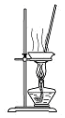 用图所示装置蒸干NaHCO3溶液制备NaHCO3晶体 | |
| C. | 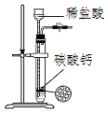 用图所示装置制取少量纯净的CO2气体 | |
| D. | 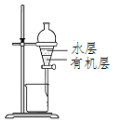 用图所示装置分离CCl4萃取碘水后的液态混合物 |
11.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法中正确的是( )
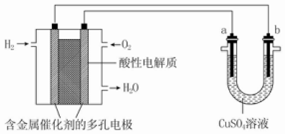

| A. | 燃料电池工作时,正极反应为 O2+2H2O+4e═4OH | |
| B. | a 极是铁,b 极是铜时,b 极逐渐溶解,a 极上有铜析出 | |
| C. | a 极是粗铜,b 极是纯铜时,a 极逐渐溶解,b 极上有铜析出 | |
| D. | a、b 两极均是石墨时,在相同条件下 a 极产生的气体与电池中消耗的 H2 体积相等 |
18.下列物质转化要加入还原剂才能实现的是( )
| A. | SO32-→SO2 | B. | SO2→S | C. | Fe2+→Fe3+ | D. | Cl2→ClO- |
15.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | SO2 | B. | Cl2 | C. | Na2CO3 | D. | CH3COOH |
13.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.3NA | |
| B. | 4.48LNH3中含原子总数目为0.8NA | |
| C. | 新制的含NA个Fe(OH)3分子的氢氧化铁胶体中,含有胶粒的物质的量为1mol | |
| D. | 23gNO2和N2O4的混合气体中含有原子总数1.5NA |