题目内容
11.用下列实验装置进行相应实验,能达到实验目的是( )| A. | 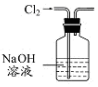 用图所示装置除去Cl2中含有的少量HCl | |
| B. | 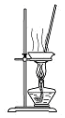 用图所示装置蒸干NaHCO3溶液制备NaHCO3晶体 | |
| C. | 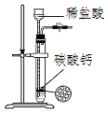 用图所示装置制取少量纯净的CO2气体 | |
| D. | 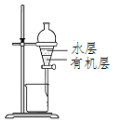 用图所示装置分离CCl4萃取碘水后的液态混合物 |
分析 A.二者均与NaOH溶液反应;
B.蒸干NaHCO3溶液时碳酸氢钠分解;
C.关闭止水夹,可使固体与液体分离,且盐酸易挥发;
D.CCl4萃取碘水后,有机层在下层,水在上层.
解答 解:A.二者均与NaOH溶液反应,应选饱和食盐水、洗气,故A错误;
B.蒸干NaHCO3溶液时碳酸氢钠分解,则不能蒸干,应选冷却结晶法,故B错误;
C.关闭止水夹,可使固体与液体分离,碳酸钙与盐酸反应生成二氧化碳,但盐酸易挥发,生成二氧化碳中混有HCl,故C错误;
D.CCl4萃取碘水后,有机层在下层,水在上层,图中分液漏斗可分离,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,把握实验装置的作用、混合物分离提纯、气体的制备实验为解答关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
2.在100℃时,水的离子积等于1.0×10-12,若该温度下某溶液中的c(H+)=1×10-7 mol/L,则该溶液( )
| A. | 呈碱性 | B. | 呈酸性 | C. | 呈中性 | D. | c(H+)=c(OH-) |
19.下列实验操作中,正确的是( )
| A. | 过滤时,用玻璃棒搅动滤纸中的液体 | |
| B. | 做钠的焰色反应实验可用玻璃棒蘸取少量NaCl的浓溶液在无色火焰上灼烧 | |
| C. | 配制溶液过程中定容摇匀后发现液面低于容量瓶的刻度线,再用胶头滴管加水至刻度线 | |
| D. | 用自来水制蒸馏水时,弃去开始馏出的部分液体 |
6.海水淡化是海岛地区提供淡水的重要手段,所谓海水淡化是指除去海水中的盐分以获得淡水的工艺过程(又称海水脱盐),其方法较多,如水合物法、电渗透法、离子交换法和压渗法等.下列方法中也可以用来进行海水淡化的是( )
| A. | 过滤法 | B. | 蒸馏法 | C. | 萃取法 | D. | 结晶法 |
16.300mL某浓度的NaOH溶液中含有60g溶质.现欲配制80mL 1mol/LNaOH溶液,应取该溶液的体积为( )
| A. | 16mL | B. | 20mL | C. | 32mL | D. | 40mL |
6.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 12g的金刚石晶体中含有碳碳键的数目为4NA | |
| B. | 46g四氧化二氮含有的原子总数一定为3NA | |
| C. | 500mLl.0mol/L的乙酸溶液中含有的H+数为0.5NA | |
| D. | 1 molFeCl3制成胶体,所得胶体的粒子数为NA |
3.下列说法错误的是( )
| A. | 钠元素性质活泼,不可能应用在电光源上 | |
| B. | 漂白粉的有效成分是Ca(ClO)2 | |
| C. | 浓硝酸可以盛放在铝制容器中 | |
| D. | 向3mL1mol/L的碳酸钠溶液中逐滴滴入稀盐酸,起初并无气体生成 |
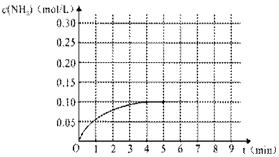 在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g )△H<0,反应中NH3的物质的量浓度的变化的情况如图:
在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g )△H<0,反应中NH3的物质的量浓度的变化的情况如图: