题目内容
某充电电池的原理如下图所示,溶液中c(H+)="2.0" mol·L-1,阴离子为SO42-,a、b均为惰性电极,充电时右槽溶液颜色由绿色(V 3+)变为紫色(V2+)。下列对此电池叙述正确的是( )
| A.充电时,b极接直流电源正极,a极接直流电源负极 |
| B.放电过程中,左槽溶液颜色由黄色变为蓝色 |
| C.充电过程中,a极的反应式为:VO2++2H++e—= VO2+ +H2O |
| D.放电时,当转移1.0 mol电子时生成1.0 mol H+,且H+从左槽迁移进右槽 |
B
解析试题分析:A、充电时右槽溶液颜色由绿色(V 3+)变为紫色(V2+),这说明右侧是得到电子的,发生还原反应,因此右侧是阴极,即充电时,b电极为阴极,a极为阳极,则b极接直流电源负极,a极接直流电源正极,A不正确;B、放电时,a电极为原电池正极,左槽中得电子发生还原反应,所以溶液颜色由黄色变为蓝色,故B正确;C、充电过程中,a极是电解池阳极,a极的电极反应式为VO2+-e-+H2O=VO2++2H+,故C错误;D、放电时,阳离子向正极移动,所以氢离子向左槽移动,故D错误,答案选B。
考点:考查原电池和电解池原理的应用和有关判断

练习册系列答案
相关题目
常见的一种锂离子电池的工作原理为LiCoO2+6C Li1-xCoO2+LixC6。下列说法正确的是
Li1-xCoO2+LixC6。下列说法正确的是
| A.充电时,阳极的电极反应式为Li1-xCoO2+xLi+xe?=LiCoO2 |
| B.充电时锂离子由阴极流向阳极 |
| C.放电时,负极的电极反应式为6C+xLi++xe-=LixC6 |
| D.放电时锂离子由负极流向正极 |
某种可充电聚合物锂离子电池放电时的反应为Li1-xCoO2 +LixC6 =" 6C" + LiCoO2,其工作原理示意图如下。下列说法不正确的是
| A.放电时LixC6发生氧化反应 |
| B.充电时,Li+通过阳离子交换膜从左向右移动 |
| C.充电时将电池的负极与外接电源的负极相连 |
| D.放电时,电池的正极反应为:Li1-xCoO2 + xLi+ + xe?= LiCoO2 |
工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。下列说法不正确的是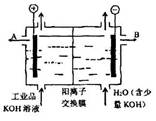
| A.阴极材料可以是Fe,含氧酸根杂质不参与电极上放电 |
| B.该电解槽的阳极反应式为:4OH―― 4e-= 2H2O+O2↑ |
| C.通电后,该电解槽阴极附近溶液pH会减小 |
| D.除去杂质后氢氧化钾溶液从出口B导出 |
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是
| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“—”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“—”、“+”极相连,Zn极质量减轻 |
按下图装置进行实验,下列描述正确的是(N装置中两个电极均为石墨棒)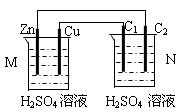
| A.C1上发生还原反应 |
| B.M 装置中SO42-移向Cu电极 |
| C.工作一段时间后装置M 中溶液pH变大,装置N中溶液pH变小 |
| D.Cu电极与C2电极上的电极反应相同 |
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是
| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“—”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“—”、“+”极相连,Zn极质量减轻 |
燃料电池是利用燃料(如H2、CO、CH4等)跟氧气反应从而将化学能转化成电能的装置。下列关于甲烷燃料电池(NaOH溶液作电解质)的说法中正确的是
| A.负极反应为:O2+2H2O+ 4e-= 4OH- |
| B.负极反应为:CH4+ 10OH-- 8e-= CO32- + 7H2O |
| C.放电时正极发生氧化反应,外电路中电子从正极流向负极 |
| D.随着放电的进行,溶液的pH保持不变 |