题目内容
在一定条件下,将钠与氧气反应的生成物1.5g溶于水,所得溶液恰好能被80mL浓度为0.50mol/L的HCl溶液中和,则该生成物的成分是( )
| A、Na2O |
| B、Na2O2 |
| C、Na2O和Na2O2 |
| D、Na2O2和NaO2 |
考点:有关混合物反应的计算,钠的化学性质
专题:
分析:由于不知道钠和氧气反应的产物为Na2O还是Na2O2或二者都有,因此可设定氧化物的化学式为Na2OX,计算出其摩尔质量,然后与两种氧化物的摩尔质量进行对比即可判断.
解答:
解:反应消耗的氯化氢的物质的量为:n(HCl)=0.08L×0.50mol/L=0.04mol,
溶液恰好能被80mL浓度为0.5mol/L的HCl溶液中和,设钠与氧气反应生成的氧化物为Na2OX,
则:Na2OX~2NaOH~2HCl
0.02mol 0.04mol
Na2OX平均摩尔质量为:M=
=75g/mol,介于Na2O(62g/mol)和Na2O2(78g/mOl)之间,
所以反应产物为Na2O和Na2O2的混合物,
故选C.
溶液恰好能被80mL浓度为0.5mol/L的HCl溶液中和,设钠与氧气反应生成的氧化物为Na2OX,
则:Na2OX~2NaOH~2HCl
0.02mol 0.04mol
Na2OX平均摩尔质量为:M=
| 1.5g |
| 0.02mol |
所以反应产物为Na2O和Na2O2的混合物,
故选C.
点评:本题考查混合物反应的计算,题目难度中等,注意明确平均摩尔质量、平均分子式在化学计算中的应用,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
如图所示,图中四种装置工作一段时间后,测得导线上均通过了0.002mol电子,此时溶液的pH由小到大的排列顺序为(不考虑溶液的水解和溶液的体积变化)( )

| A、①<②<③<④ |
| B、②<①<③<④ |
| C、②<①<④<③ |
| D、①<②<④<③ |
下列关于电子式的说法不正确的是( )
| A、每种元素的原子都可以写出电子式 |
| B、简单阳离子的电子式与它的离子符号相同 |
| C、阴离子的电子式要加方括号表示 |
| D、电子式就是核外电子排布的式子 |
下列实验不能达到实验目的是( )
| A、用CaCl2溶液可区别Na2C03和NaHCO3溶液 |
| B、用CC14萃取碘水中的碘 |
| C、用饱和NaHCO3溶液除去C02中的HCl |
| D、检验未知溶液是否含S042-,可先加氯化钡,再加稀盐酸 |
将0.1mol两种气态烃组成的混合气体完全燃烧后得到3.36L(标准状况)CO2和3.6gH2O,下列说法正确的是( )
| A、一定有乙烯 |
| B、一定有甲烷 |
| C、一定没有甲烷 |
| D、一定没有乙烷 |
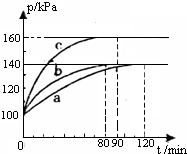 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下.
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g),反应过程如下. 煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
