��Ŀ����
18���̷���FeSO4•7H2O��������ȱ����ƶѪ����Чҩ������������Ʒ��������м���������������ʣ������̷���һ�ַ�����
��֪����H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5��
�ش��������⣺
��1�����������̷��������Ƿ���Fe3+��ʵ�������ȡ������������ˮ���μ�KSCN��Һ����������Ѫ��ɫ������������Fe3+��
��2������������Һ���������ữ��pH=2��Ŀ����ʹSn2+��ȫ���SnS��������Fe2+��������ͨ�����������͵�Ŀ���ǣ��˿ղ��
�ٳ�ȥ����I������Һ�к��е�Sn2+���������ӣ�
�ڷ�ֹFe2+��������
��3������IV��˳������Ϊ���������ᾧ�����ˡ�ϴ�ӣ�
��4������IV�õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ�
�ٳ�ȥ������渽�ŵ���������ʣ��ڽ���ϴ�ӹ�����FeSO4•7H2O����ģ�
��5���ⶨ�̷���Ʒ��Fe2+�����ķ����ǣ�
a����ȡ2.8500g�̷���Ʒ���ܽ⣬��250mL����ƿ�ж��ݣ�
b����ȡ25.00mL������Һ����ƿ�У�
c���������ữ��0.01000mol/L KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00mL���ζ�ʱ������Ӧ�����ӷ���ʽΪ��5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O����
�ټ���������Ʒ��FeSO4•7H2O����������Ϊ97.54%��
���������������ⶨ����Ʒ��FeSO4•7H2O����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ��������ԭ������Ʒ�д������������ʣ���H2O��H2SO4�ȣ�����Ʒ���ֱ�������
���� ��м����ϡ�����������������������������˺�õ���Һ������Һ����ϡ�����ữ����ͨ�����⣬������SnS��������ֹ�������ӱ����������˺�õ���ҺΪ����������������Ũ���ᡢ��ȴ�ᾧ�����˿ɵõ�FeSO4•7H2O��
��1���������������ӵļ��鷽�������ش����������������������Һ��Ѫ��ɫ��
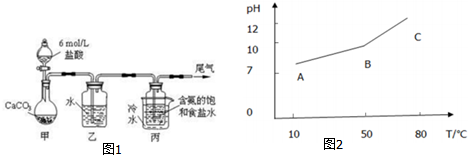
��2���������̹�ϵͼ��������H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0�����������ϡ���������ҺPH=2Ϊ�˳�ȥ��������Sn2+��ͨ�������Ʊ��ͣ�������ǿ��ԭ����Ŀ���dz��������ӣ���ֹ�������ӱ�������
��3������IV��Ŀ���Ǵ���Һ�������̷����壬��������Ũ�����ᾧϴ�ӵõ����壻
��4������IV�õ����̷�������������ˮϴ��Ŀ����ϴȥ�������ʣ��¶Ƚ����̷��ܽ�Ƚ��ͣ������̷��������ʧ��
��5�����ݵζ�ʵ��ķ�Ӧ�յ�ʱ�����ķ�Ӧ���м��㣬����ʵ������в��������������������жϣ�
��� �⣺��1�����������̷��������Ƿ���Fe3+��ʵ��������������������Ӽ��鷽������������������������������ӻᷴӦ������������Ѫ��ɫ��֤�������ӵĴ��ڣ�
�ʴ�Ϊ��ȡ������������ˮ���μ�KSCN��Һ����������Ѫ��ɫ������������Fe3+��
��2����֪����H2S������Һ�У�SnS������ȫʱ��Һ��pHΪ1.6��FeS��ʼ����ʱ��Һ��pHΪ3.0��������ȫʱ��pHΪ5.5������������Һ���������ữ��pH=2��Ŀ���ǣ�����ҺPH=2ʱ��Sn2+��ȫ�������������Ӳ�������ͨ�����������͵�Ŀ���ǣ��������ǿ��ԭ�ԣ����Է�ֹ�������ӱ�������
�ʴ�Ϊ��ʹSn2+��ȫ���SnS��������Fe2+����������ֹFe2+��������
��3����Һ�еõ����壬��Ҫ����Һ���м�������Ũ�����ᾧ����������ϴ�ӵȣ����Բ���IV��˳������Ϊ���������ᾧ�����ˡ�ϴ�ӣ�
�ʴ�Ϊ���������ᾧ�����ˡ�ϴ�ӣ�
��4����ˮ�¶ȵͣ������ܽ�ȼ�С������ϴȥ����������������ӣ������̷��ܽ��������ʧ��
�ʴ�Ϊ������ϴ�ӹ�����FeSO4•7H2O����ģ�
��5����a����ȡ2.8500g�̷���Ʒ���ܽ⣬��250mL����ƿ�ж��ݣ�
b����ȡ25.00mL������Һ����ƿ�У�
c���������ữ��0.01000mol/L KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00mL�����ݷ�Ӧ����ʽ���㣺
5Fe2++MnO4-+8H+�T5Fe3++Mn2++4H2O
5 1
n��Fe2+�� 0.01000mol/L��0.0200L
����õ���n��Fe2+��=0.001mol��
��250mL��Һ�к�Fe2+=0.001mol��$\frac{250}{25}$=0.01mol��
FeSO4•7H2O���ʵ���Ϊ0.01mol������=0.01mol��278g/mol=2.78g��
��������=$\frac{2.78g}{2.85g}$��100%=97.54%��
�ʴ�Ϊ��97.54%��
�������������ⶨ��Ʒ��FeSO4•7H2O����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ�������ԭ����ϴ�Ӳ����ף��������ӱ������е���������������
�ʴ�Ϊ����Ʒ�д������������ʣ���H2O��H2SO4�ȣ�����Ʒ���ֱ�������
���� ���⿼�������Ʊ��������̣��漰���ʵķ����ᴿ����ԭ���ķ������ۡ��������ơ����ʺ����ⶨ�ȣ�ע�����Ŀ��Ϣ���ã���������Ԫ�ػ�����֪ʶ������������ѧ������������ʵ���������Ѷ��е�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д� �����ܱ������п��淴ӦA2��g��+3B2��g��?2AB3��g����̽����һ�����ı�����£���������ƽ��״̬�ĸı䣬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ����������ж���ȷ���ǣ�������
�����ܱ������п��淴ӦA2��g��+3B2��g��?2AB3��g����̽����һ�����ı�����£���������ƽ��״̬�ĸı䣬�õ���ͼ��ʾ�����ߣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ����������ж���ȷ���ǣ�������| A�� | �����������ʹ״̬d��Ϊ״̬b | |
| B�� | ��T1��T2�����淴Ӧһ���Ƿ��ȷ�Ӧ | |
| C�� | �ﵽƽ��ʱA2��ת���ʴ�СΪ��b��a��c | |
| D�� | ��T2��n��A2������ʱ�ﵽƽ�⣬AB3�����ʵ�����СΪ��c��b��a |
| A�� | ϡ�������ͭƬ�ϣ�Cu+2H+�TCu2++H2 | |
| B�� | ����ͭ�����ᷴӦ��O2-+2 H+�TH2O | |
| C�� | �����ƺ��Ȼ���������Һ��ϣ�Ba2++SO42-�TBaSO4�� | |
| D�� | ������ʯ��ʯ��Ӧ��CaCO3+2H+�TCa2++H2O+CO2�� |
| A�� | ϡ�����������м��Ӧ��Fe+4H++NO3-�TFe3++NO��+2H2O | |
| B�� | ̼������Һˮ������ӷ���ʽ��CO32-+2H2O?H2CO3+2OH- | |
| C�� | ������ȼ����Ϊ285.8 kJ/mol�����ʾ����ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��g����H=-571.6 kJ/mol | |
| D�� | Ũ������MnO2������������MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O |
| Ԫ�ش��� | A | B | C | D | E |
| ԭ�Ӱ뾶/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | -1 | -2 |
��2��C���⻯��ĵ���ʽΪ
 ��
����3��B������������ˮ������C������������ˮ���ﷴӦ�����ӷ���ʽΪ��Al��OH��3+3H+=Al3+3H2O��
��4����������Ԫ�ص�����������Ӧˮ�����������ǿ����HClO4���ѧʽ����
��5��C��E�γɵĻ�����ΪSO2��SO3���ѧʽ��
��6���õ���ʽ��ʾAD�γɻ�����Ĺ��̣�
 ��
�� 
 ��֪��A��B��C��D��E��F����Ԫ�غ˵�������������������ڱ���ǰ�����ڵ�Ԫ�أ�����Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�CԪ���ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ���������ߵģ�Fԭ�Ӻ���������������B��ͬ���������������������������Ϣ���ش��������⣺
��֪��A��B��C��D��E��F����Ԫ�غ˵�������������������ڱ���ǰ�����ڵ�Ԫ�أ�����Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�CԪ���ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵ��۵���ͬ����Ԫ���γɵĵ���������ߵģ�Fԭ�Ӻ���������������B��ͬ���������������������������Ϣ���ش��������⣺