题目内容
8.一定量的无水酒精完全燃烧时放出的热量为Q,它所生成的CO2用过量饱和石灰水完全吸收可得100g CaCO3沉淀,则完全燃烧46g无水酒精时放出的热量是( )| A. | 0.5Q | B. | 5Q | C. | 2Q | D. | Q |
分析 利用生成的CO2用过量饱和石灰水完全吸收,可得100克CaCO3沉淀可计算出二氧化碳的物质的量,即得出二氧化碳的物质的量与放出的热量的关系,再利用完全燃烧1摩尔无水乙醇生成2摩尔二氧化碳来分析放出的热量.
解答 解:因生成的CO2用过量饱和石灰水完全吸收,可得100克CaCO3沉淀,
CaCO3的物质的量为$\frac{100g}{100g/mol}$=1mol,
由碳元素守恒可知,二氧化碳的物质的量也为1mol,
即生成1mol二氧化碳放出的热量为Q,
而完全燃烧1摩尔无水乙醇时生成2mol二氧化碳,
则放出的热量为Q×2=2Q,
故选:C.
点评 本题考查学生利用化学反应中的元素守恒来分析二氧化碳的量及二氧化碳的量与放出的热量的关系,明确物质的物质的量与热量成正比是解答本题的关键.

练习册系列答案
相关题目
19.日常所用锌-锰干电池的电极分别为锌筒和石墨棒,以糊状NH4Cl作电解质,电极反应为:Zn-2e-=Zn2+,2MnO2+2NH4++2e-=Mn2O3+2NH3+H2O.下列有关锌-锰干电池的叙述中,正确的是( )
| A. | 干电池中锌筒为正极,石墨棒为负极 | |
| B. | 干电池长时间连续工作后,糊状物可能流出,腐蚀用电器 | |
| C. | 干电池工作时,电流方向是由锌筒经外电路流向石墨棒 | |
| D. | 干电池可实现化学能向电能和电能向化学能的相互转化 |
16.化学反应是旧化学键断裂和新化学键形成的过程.氢气与氧气的反应中,破坏lmol氢氢键消耗的能量为Q1kJ、破坏1mol氧氧键消耗的能量为Q2kJ、形成lmol氢氧键释放的能量为Q3kJ.下列关系中正确的是( )
| A. | Ql+Q2<Q3 | B. | Ql+Q2>2Q3 | C. | 2Ql+Q2<4Q3 | D. | 2Ql+Q2>4Q3 |
3.气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成( )
| A. | NH4C1 | B. | NH4HCO3 | C. | (NH4)2CO3 | D. | (NH4)2SO4 |
20.下列说法中不正确的是( )
| A. | 化石燃料在燃烧过程中会产生污染环境的CO、SO2等有害气体 | |
| B. | 直接燃烧煤不如将煤进行深加工后再燃烧的效果好 | |
| C. | 太阳能、氢能、风能、核能、天然气等都属于新能源 | |
| D. | 水煤气是一种二次能源,比煤直接燃烧污染小 |
17.下列关于有机物的叙述不正确的是( )
| A. | 甲烷、甲苯、乙醇、乙酸都可以发生取代反应 | |
| B. | 能发生银镜反应的有机物都是醛 | |
| C. | 乙酸乙酯在无机酸或碱存在时都能发生水解反应 | |
| D. | 可用浓溴水来区分乙醇和苯酚 |
18.已知某含苯环的分子C8H10,苯环上有两个侧链,其一氯取代物的种数是(不考虑立体异构)( )
| A. | 10种 | B. | 9种 | C. | 6种 | D. | 5种 |
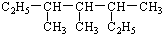 3,4,5-三甲基庚烷
3,4,5-三甲基庚烷

 B.
B.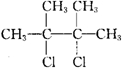 C.
C. .
.