题目内容
下列说法中正确的是( )
| A.[Cu(NH3)4]2+和CH4两个粒子中中心原子Cu和C都是通过sp3杂化轨道成键 |
| B.气体单质中,一定有σ键,可能有π键 |
| C.两个原子之间形成共价键时,最多有一个σ键 |
| D.中心原子采用sp2,该分子一定是平面三角形 |
A..[Cu(NH3)4]2+中的Cu是dsp2杂化,CH4中中心原子C是通过sp3杂化轨道成键,故A错误;
B.气体单质中不一定含有σ键,如稀有气体是单原子分子,不存在化学键,只存在范德华力,故B错误;
C.因为δ键是头碰头形成的,一个方向上只可能有一个杂化轨道,所以最多有一个σ键,故C正确;
D.中心原子采用sp2,该分子不一定是平面三角形,如CH2=CH2中碳原子采取SP2杂化,但乙烯是平面型结构,故D错误;
故选C.
B.气体单质中不一定含有σ键,如稀有气体是单原子分子,不存在化学键,只存在范德华力,故B错误;
C.因为δ键是头碰头形成的,一个方向上只可能有一个杂化轨道,所以最多有一个σ键,故C正确;
D.中心原子采用sp2,该分子不一定是平面三角形,如CH2=CH2中碳原子采取SP2杂化,但乙烯是平面型结构,故D错误;
故选C.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、进行钠的有关性质实验时,用剩的钠应放回原试剂瓶 | B、常用25.00 ml 碱式滴定管准确量取20.00 ml KMnO4溶液 | C、用湿润的淀粉碘化钾试纸可以鉴别NO2和Br2蒸气 | D、某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- |
Na3N和NaH都是离子化合物,与水反应都有气体生成,下列说法中正确的是( )
| A、两种物质的阴离子半径都比阳离子半径小 | B、溶于水,所得溶液都能使无色酚酞变红 | C、与水反应时,水都做氧化剂 | D、与盐酸反应都只生成一种盐 |
下列说法中正确的是( )
| A、用碱石灰除去氯气中的水 | B、碘化银是重要的感光材料,溴化银可用于人工降雨 | C、过氧化钠可用作潜艇里氧气的来源 | D、焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
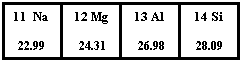 如图为元素周期表第三周期的一部分.据此判断下列说法中正确的是( )
如图为元素周期表第三周期的一部分.据此判断下列说法中正确的是( )| A、Si元素的名称是硅,其核电荷数为14 | B、Mg原子的结构示意图是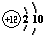 | C、Al的相对原子质量是26.98g | D、它们都属于金属元素 |
下列说法中正确的是( )
| A、O、Na、S元素的原子半径依次增大 | B、KOH、Mg(OH)2、Ba(OH)2的碱性依次增强 | C、H2SO4、H3PO4、HClO4的酸性依次增强 | D、F2、Cl2、Br2、I2的氧化性依次减弱 |