题目内容
17.在原子序数为1~18号元素中,请用化学式填写.(1)与水反应最剧烈的金属元素是Na;
(2)元素的气态氢化物最稳定的物质是HF;
(3)元素的最高价氧化物所对应的水化物酸性最强的物是HClO4.
分析 (1)金属性越强与水反应越剧烈;
(2)非金属性越强,对应氢化物越稳定;
(3)根据铜同周期从左向右最高价氧化物对应水化物的酸性越来越强,同主族从上向下最高价氧化物对应水化物的酸性越来越弱,则在前三个周期中,最高价氧化物对应水化物的酸性最强的元素是Cl(不是F,因为F无最高正价).
解答 (1)同周期金属性减弱,同主族金属性增强,与水反应最剧烈的金属元素是Na;故答案为:Na;
(2)非金属性越强,对应氢化物越稳定,1~18号元素中氟的非金属性最强,所以HF最稳定,故答案为:HF;
(3)根据铜同周期从左向右最高价氧化物对应水化物的酸性越来越强,同主族从上向下最高价氧化物对应水化物的酸性越来越弱,则在前三个周期中,最高价氧化物对应水化物的酸性最强的元素是Cl(不是F,因为F无最高正价),故答案为:HClO4.
点评 本题考查了基本递变规律,是解决问题的基础知识,问题不难,但要熟练运用和灵活运用却不容易,因此,一定要熟记这些知识.

练习册系列答案
相关题目
12.在恒容条件下,能使反应NO2 (g)+CO(g)?NO(g)+CO2(g)的反应速率增大且活化分子的百分数也增大的措施是( )
| A. | 增大 NO2或CO的浓度 | B. | 减小 NO或CO2的浓度 | ||
| C. | 通入Ne使气体的压强增大 | D. | 升高反应温度 |
9.设NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标准状况下,2.24LSO3所含分子数为0.1NA | |
| B. | 0.1 mol Fe与足量盐酸反应,转移的电子数为0.3 NA | |
| C. | 1molNa2O2与足量水反应转移的电子数为NA | |
| D. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
6.中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,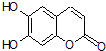 氢原子未画出),具有抗菌作用.若1mol七叶树内酯与NaOH溶液完全反应,则消耗的NaOH的物质的量为( )
氢原子未画出),具有抗菌作用.若1mol七叶树内酯与NaOH溶液完全反应,则消耗的NaOH的物质的量为( )
 氢原子未画出),具有抗菌作用.若1mol七叶树内酯与NaOH溶液完全反应,则消耗的NaOH的物质的量为( )
氢原子未画出),具有抗菌作用.若1mol七叶树内酯与NaOH溶液完全反应,则消耗的NaOH的物质的量为( )| A. | 2 mol | B. | 3 mol | C. | 4 mol | D. | 1mol |
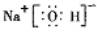 .
.
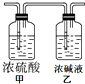 某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求
某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求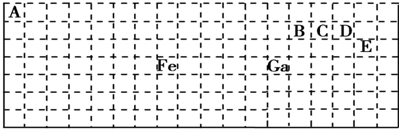
 .
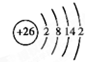
.
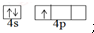
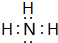 ,含有共价键化学键,E的电子表达式是
,含有共价键化学键,E的电子表达式是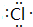 .
.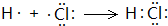 .
.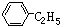

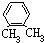
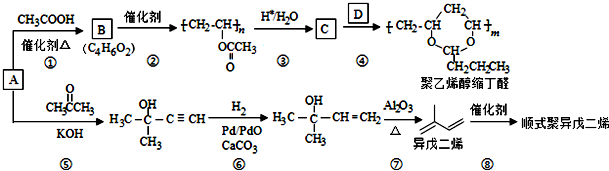
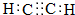 ,B含有的含氧官能团是酯基(写名称).
,B含有的含氧官能团是酯基(写名称).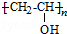 ,D为CH3CH2CH2CHO.
,D为CH3CH2CH2CHO. .
.