题目内容
20. 硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图,该电池工作时反应为:4VB2+11O2→4B2O3+2V2O5.下列说法正确的是( )
硼化钒(VB2)-空气电池是目前储电能力最高的电池,电池示意图如图,该电池工作时反应为:4VB2+11O2→4B2O3+2V2O5.下列说法正确的是( )| A. | 电极a为电池负极,发生还原反应 | |
| B. | 每消耗1mol VB2转移6mol电子 | |
| C. | 电池工作时,OH-向电极a移动 | |
| D. | VB2极发生的电极反应为:2VB2+22OH--22e-→V2O5+2B2O3+11H2O |
分析 硼化钒(VB2)-空气电池中,电池总反应为:4VB2+11O2→4B2O3+2V2O5,VB2在负极失电子,氧气在正极上得电子,电子从负极流向正极,据此分析.
解答 解:A、硼化钒(VB2)-空气电池中,VB2在负极失电子,氧气在正极上得电子,所以a为正极,发生还原反应,故A错误;
B、根据2VB2+22OH--22e-═V2O5+2B2O3+11H2O,每消耗1mol VB2 转移11mol电子,故B错误;
C、该电池正极产生氢氧根离子,负极消耗氢氧根离子,阴离子向负极移动,而a为正极,故C错误;
D、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O,故D正确.
故选D.
点评 本题考查原电池的工作原理,题目难度中等,本题注意把握电极的判断方法和电极反应式的书写以及正确判断离子的定向移动和计算.

练习册系列答案
相关题目
11.明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,…冷定,毁罐取出,…,即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭).下列说法不正确的是( )
| A. | 倭铅是指金属锌和铅的混合物 | |
| B. | 煤炭中起作用的主要成分是C | |
| C. | 冶炼Zn的过程中有氧化还原反应发生 | |
| D. | 该冶炼锌的方法属于热还原法 |
8.短周期元素X、Y、Z、W、R的化合价与原子序数的关系如图所示.下列说法正确的是( )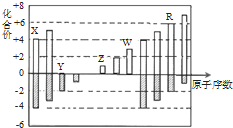

| A. | 原子半径:Z>Y>X | |
| B. | Z和Y形成的化合物是离子化合物 | |
| C. | 气态氢化物的稳定性:Y<R | |
| D. | 常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液 |
15.下列有关物质性质的应用正确的是( )
| A. | 水中加入明矾,可以起到杀菌消毒的作用 | |
| B. | 氧化铝中加入冰晶石,可以起到降低熔点的作用 | |
| C. | 药皂中加入少量苯酚,可以起到增白去污的作用 | |
| D. | 食品包装袋中放入生石灰,可以起到防止月饼等富脂食品氧化变质的作用 |
5.下列关于化学用语的表示正确的是( )
| A. | 质子数为8、中子数为10的氧原子:${\;}_{8}^{10}$O | |
| B. | 氯离子的结构示意图: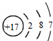 | |
| C. | 对苯二甲酸的结构简式: | |
| D. | NaHCO3在水溶液中的电离方程式:NaHCO3=Na++HCO3- |
12.下列指定反应的离子方程式正确的是( )
| A. | NO2溶于水:3NO2+H2O=2H++2NO3-+NO↑ | |
| B. | 用氨水吸收足量的SO2气体:2OH-+SO2=SO32-+H2O | |
| C. | 溴乙烷与氢氧化钠水溶液共热:C2H5Br+OH-$→_{△}^{H_{2}O}$ CH2=CH2↑+Br-+H2O | |
| D. | 用酸性K2Cr2O7溶液检验酒精:3CH3CH2OH+2Cr2O72-+2H2O=4Cr(OH)3↓+3CH3COO-+OH- |
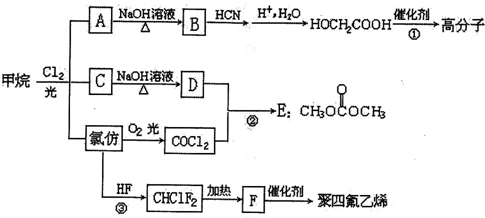
9. 如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述错误的是( )
如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述错误的是( )
 如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述错误的是( )
如图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基).则下列有关叙述错误的是( )| A. | 反应①属于加成反应 | |
| B. | W能发生加成、水解、氧化反应 | |
| C. | X在一定条件下可发生缩聚反应 | |
| D. | 一定条件下Z与足量H2反应后所得产物中至少含有4个手性碳原子 |
 .
.

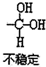 $\stackrel{自动}{→}$
$\stackrel{自动}{→}$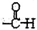
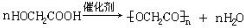 ②
②