题目内容
在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量
⑤混合气体总质量 ⑥2v(B)正=v(C)逆 ⑦当有2molB生成的同时有1molC生成.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量
⑤混合气体总质量 ⑥2v(B)正=v(C)逆 ⑦当有2molB生成的同时有1molC生成.
| A、②③⑤⑦ | B、①②③⑥ |
| C、②③④⑥ | D、①③④⑤⑦ |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:反应到达平衡状态时,正逆反应速率相等,平衡时各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,由此进行判断.
解答:
解:①该反应是反应前后气体体积没有变化的反应,所以容器中的压强不再发生变化,不能证明达到了平衡状态,故①错误;
②该容器的体积保持不变,根据质量守恒定律知,反应前后混合气体的质量会变,所以当混合气体的密度不再发生变化时,能表明达到化学平衡状态,故②正确;
③反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的浓度等不再发生变化,所以各气体物质的物质的量浓度不再变化时,该反应达到平衡状态,故③正确;
④该反应是反应前后气体体积没有变化的反应,所以气体总物质的量不变,不能表明反应达到平衡状态,故④错误;
⑤未平衡时总质量是变化的,现在不变说明达平衡状态,故⑤正确;
⑥2v(B)正=4v(C)正=v(C)逆,故⑥错误;
⑦当有2molB生成等效于1molC消耗同时有1molC生成,故⑦正确;
故选A.
②该容器的体积保持不变,根据质量守恒定律知,反应前后混合气体的质量会变,所以当混合气体的密度不再发生变化时,能表明达到化学平衡状态,故②正确;
③反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的浓度等不再发生变化,所以各气体物质的物质的量浓度不再变化时,该反应达到平衡状态,故③正确;
④该反应是反应前后气体体积没有变化的反应,所以气体总物质的量不变,不能表明反应达到平衡状态,故④错误;
⑤未平衡时总质量是变化的,现在不变说明达平衡状态,故⑤正确;
⑥2v(B)正=4v(C)正=v(C)逆,故⑥错误;
⑦当有2molB生成等效于1molC消耗同时有1molC生成,故⑦正确;
故选A.
点评:本题考查化学平衡状态的判断,难度不大,注意只有反应前后不相同的量才能作为判断化学平衡的依据,反应前后不改变的量不能作为判断化学平衡的依据,如该反应中的压强就不能作为判断化学平衡的依据.

练习册系列答案
相关题目
在下列实验操作中错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计的水银球放置于蒸馏烧瓶的支管出口稍下处 |
| C、用容量瓶配制溶液时,加水超过了刻度线,没有采取补救措施,重新配制 |
| D、将5.85gNaCl溶于100mL水中,即配成1.0 mol/L NaCl溶液 |
下列化合物中,既有离子键,又有共价键的是( )
| A、CaO |
| B、SiO2 |
| C、H2O |
| D、Na2O2 |
化合物丙可由如图反应得到:丙的结构不可能是( )
C4H10O(甲)
C4H8
(乙) C4H8Br2(丙)
C4H10O(甲)
| 浓H2SO4 |
| △ |
| Br2 |
| CCl4 |
| A、CH3CBr2CH2CH3 |
| B、(CH3)2CBrCH2Br |
| C、C2H5CHBrCH2Br |
| D、CH3(CHBr)2CH3 |
NA表示阿伏加德罗常数的值,下列说法一定正确的是( )
| A、7.8g Na2S和Na2O2的混合物中含有的离子总数为0.3NA |
| B、将1mol KClO3和SO3的混合物溶于水,溶液中自由移动的离子数目为3NA |
| C、标准状况下,22.4L氯气与足量的铁反应,转移电子数为0.2 NA |
| D、常温常压下,将0.1mol氯气通入水中发生化学反应,转移电子数为0.1 NA |
下列各组粒子中属于同位素的是( )
| A、24Mg和24Na |
| B、H2O和D2O |
| C、H2和D2 |
| D、16O和18O |
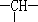 和一个-Cl,它可能的结构有
和一个-Cl,它可能的结构有